摘要:9.在一定条件下.不能与SiO2反应的是( ) ①焦炭 ②SO2 ③CaO ④氢氟酸 ⑤H2O ⑥KOH ⑦Na2CO3 ⑧浓硫酸 A.③⑤⑦ B.⑤⑦⑧ C.②⑤⑧ D.只有⑧
网址:http://m.1010jiajiao.com/timu3_id_188255[举报]
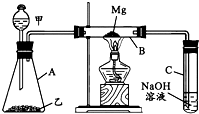 某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答:
某研究性学习小组认为SiO2、SO2和CO2都是酸性氧化物,化学性质应具有一定的相似性,他们以课本知识“Mg在点燃的条件下可与CO2反应”为基础,设计了如图所示装置进行Mg和SO2反应的实验.据此请回答:(1)若用下列物质中的两种相互混合反应制取SO2,则这两种物质最好是
②③
②③
(填代号).①10%的H2SO4溶液
②50%的H2SO4溶液
③Na2SO3固体
④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式
2Mg+SO2
2MgO+S,Mg+S
MgS
| ||
| ||
2Mg+SO2
2MgO+S,Mg+S
MgS
.装置C中NaOH溶液的作用是
| ||
| ||
吸收多余的SO2,防止污染环境
吸收多余的SO2,防止污染环境
.(3)你认为该装置是否有不足之处?如果有,请说明之.答:
有 在A和B之间未连接一干燥装置;C装置未与大气相通;在镁下方未垫一不锈钢片,镁能与玻璃管反应;没有防倒吸装置
有 在A和B之间未连接一干燥装置;C装置未与大气相通;在镁下方未垫一不锈钢片,镁能与玻璃管反应;没有防倒吸装置
.(4)有同学认为,B管中的生成物中含有MgS,请你设计实验方案加以证明.答:
可加入稀硫酸,发生:MgS+H2SO4=MgSO4+H2S↑,H2S具有臭鸡蛋气味.
可加入稀硫酸,发生:MgS+H2SO4=MgSO4+H2S↑,H2S具有臭鸡蛋气味.
.(附加题)X、Y、Z为常见的三种单质,Z是绿色植物光合作用的产物之一,A、B为常见化合物.它们在一定条件下可发生如图所示的反应(均是在非溶液中进行的反应):

(1)当X为金属,Y为非金属时,A是
(2)当X为非金属,Y为金属时,X可能是
(3)当X与Y均为金属时,X与A反应的化学方程式是
(4)当X与Y均为非金属时,若X与Y同主族,X与A反应的化学方程式是
查看习题详情和答案>>

(1)当X为金属,Y为非金属时,A是
镁
镁
(填名称).(2)当X为非金属,Y为金属时,X可能是
H2
H2
或C
C
(均填化学式).(3)当X与Y均为金属时,X与A反应的化学方程式是
8Al+3Fe3O4
9Fe+4Al2O3(或2Al+Fe2O3
2Fe+Al2O3)
| ||
| ||
8Al+3Fe3O4
9Fe+4Al2O3(或2Al+Fe2O3
2Fe+Al2O3)
.
| ||
| ||
(4)当X与Y均为非金属时,若X与Y同主族,X与A反应的化学方程式是
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
.若X与Y不在同一主族,X与A反应的化学方程式是
| ||
C+H2O
H2+CO
| ||
C+H2O
H2+CO
.
| ||
(18分)运用物质结构的知识完成下列问题。
(1)第一电离能介于B、N之间的第二周期元素有 (填元素符号)。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ,配体的化学式为 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
Q R
①晶体Q中不存在的作用力为 (填字母)。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
②R中阳离子的空间构型为 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如下图3所示。则m= (填数字)。
(5)以四氯化钛、碳化钙、叠氮酸盐(如NaN3)作原料,可以生成碳氮化钛化合物,其结构是用碳原子取代氮化钛晶胞(结构如下图4)所有顶点的氮原子,这种碳氮化钛化合物的化学式为 。

图3 图4
(6)部分化学键的键能见下表:
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
②工业上高纯硅可通过下列反应制取:SiCl4 (g) + 2H2(g) 高温Si(s) + 4HCl(g)
计算该反应的反应热△H =___________ kJ/mol。 查看习题详情和答案>>
(18分)运用物质结构的知识完成下列问题。
(1)第一电离能介于B、N之间的第二周期元素有 (填元素符号)。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ,配体的化学式为 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

Q R
①晶体Q中不存在的作用力为 (填字母)。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
②R中阳离子的空间构型为 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如下图3所示。则m= (填数字)。
(5)以四氯化钛、碳化钙、叠氮酸盐(如NaN3)作原料,可以生成碳氮化钛化合物,其结构是用碳原子取代氮化钛晶胞(结构如下图4)所有顶点的氮原子,这种碳氮化钛化合物的化学式为 。


图3 图4
(6)部分化学键的键能见下表:
①比较下列两组物质的熔点高低 (填“>”或“<”) SiC______ Si; SiCl4 ______ SiO2
②工业上高纯硅可通过下列反应制取:SiCl4 (g) + 2H2(g) 高温Si(s) + 4HCl(g)
计算该反应的反应热△H =___________ kJ/mol。
(1)第一电离能介于B、N之间的第二周期元素有 (填元素符号)。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ,配体的化学式为 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

Q R
①晶体Q中不存在的作用力为 (填字母)。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
②R中阳离子的空间构型为 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如下图3所示。则m= (填数字)。
(5)以四氯化钛、碳化钙、叠氮酸盐(如NaN3)作原料,可以生成碳氮化钛化合物,其结构是用碳原子取代氮化钛晶胞(结构如下图4)所有顶点的氮原子,这种碳氮化钛化合物的化学式为 。


图3 图4
(6)部分化学键的键能见下表:
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
②工业上高纯硅可通过下列反应制取:SiCl4 (g) + 2H2(g) 高温Si(s) + 4HCl(g)
计算该反应的反应热△H =___________ kJ/mol。