摘要:(1)可能是H+使CuO溶解 Na2SO4溶液 不溶解 (4)稀硫酸中的H+使CuO溶解 (5)2Cu+O2 加热 2CuO CuO+H2SO4=CuSO4+H2O 将试管放在酒精灯上加热至铜镜变黑后.加入稀硫酸充分反应即可
网址:http://m.1010jiajiao.com/timu3_id_18770[举报]
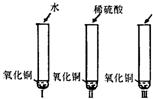 28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.
28、氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H+、SO42-、H2O)能使氧化铜溶解,请你帮他通过下图中的三个实验完成探究活动.【提出假设】你提出的假设是
稀H2SO4中的H+溶解CuO
.【设计实验】通过实验Ⅰ可证明
水不能溶解CuO
.要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和实验Ⅲ,在实验皿中应加入
稀盐酸或Na2SO4或硫酸钾或硫酸铜
【实验结果】探究结果为
稀H2SO4中的H+溶解CuO,H2O和SO42-不能溶解CuO
.请写出氧化铜与稀硫酸反应的化学方程式:
CuO+H2SO4═CuSO4+H2O
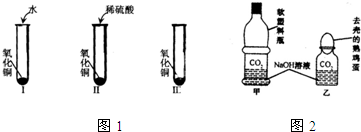
.(1)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解.请你和他一起通过图1中I、Ⅱ、Ⅲ三个实验完成这次探究活动.
①你提出的假设是
②通过实验I可证明
③要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入
④探究结果为
(2)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?
①我设计了甲、乙两个实验来验证,如图所示,实验现象为:甲-软塑料瓶变瘪,乙-“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是:
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:
我思考后,又补充了一个实验来回答,这个实验是:
②小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
写出方案2中所涉及的化学方程式
查看习题详情和答案>>

①你提出的假设是
可能是H+使CuO溶解
可能是H+使CuO溶解
.②通过实验I可证明
水不能溶解CuO
水不能溶解CuO
.③要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入
Na2SO4溶液
Na2SO4溶液
.④探究结果为
稀硫酸中的H+使CuO溶解
稀硫酸中的H+使CuO溶解
.你认为除实验Ⅱ和Ⅲ所用试剂外,还能够溶解氧化铜的一种常见物质是稀盐酸或稀硝酸等
稀盐酸或稀硝酸等
.(2)化学复习课上,老师将CO2分别通入澄清的石灰水和NaOH溶液中,我们观察到前者变浑浊,后者无明显现象,CO2和NaOH是否确实发生了化学反应?
①我设计了甲、乙两个实验来验证,如图所示,实验现象为:甲-软塑料瓶变瘪,乙-“瓶吞鸡蛋”.
小虎同学认为上述实验是可行的,其共同原理是:
稀硫酸中的H+使CuO溶解
稀硫酸中的H+使CuO溶解
小余同学提出了质疑,他认为上述实验还不足以证明CO2与NaOH确实发生了反应,其理由是:
在密闭的体系里消耗CO2,使气体压强减小;NaOH溶液中有水,CO2又能溶于水且可以与水反应
在密闭的体系里消耗CO2,使气体压强减小;NaOH溶液中有水,CO2又能溶于水且可以与水反应
_;我思考后,又补充了一个实验来回答,这个实验是:
取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度;
取一个与甲装置同样大小和质地的软塑料瓶,充满CO2后,注入与NaOH溶液体积相同的水,振荡,比较瓶子变瘪的程度;
.②小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
| 实验步骤和方法 | 实验现象 | 实验结论 | |
| 方案1 | 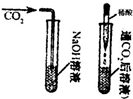 |
① 有气泡产生 有气泡产生 |
CO2和NaOH确实发生了化学反应 |
| 方案2 | ② 将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液【或石灰水或BaCl2溶液或Ba(OH)2溶液】【也可仿照方案一的图示】 将CO2通入NaOH溶液后,再向溶液中滴加CaCl2溶液【或石灰水或BaCl2溶液或Ba(OH)2溶液】【也可仿照方案一的图示】 |
③ 出现白色浑浊(或产生白色沉淀) 出现白色浑浊(或产生白色沉淀) |
CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl
CO2+2NaOH═Na2CO3+H2O,Na2CO3+CaCl2═CaCO3↓+2NaCl
.