摘要:12.Se(硒)是第四周期的VIA族元素.根据元素周期表和元素周期律分析.以下说法中错误的是 A.Se能形成SeO2 .SeO3两种氧化物 B.原子半径:Se>S C.H2Se比H2S稳定 D.酸性:H2SeO4比H2SO4弱
网址:http://m.1010jiajiao.com/timu3_id_187535[举报]
|
Se(硒)是第四周期的ⅥA族元素,根据元素周期表和元素周期律分析,以下说法中错误的是 | |
| [ ] | |
A. |
Se能形成SeO2、SeO3两种氧化物 |
B. |
原子半径:Se>S |
C. |
H2Se比H2S稳定 |
D. |
酸性:H2SeO4比H2SO4弱 |
Se(硒)是第四周期的ⅥA族元素,根据元素周期表和元素周期律分析,以下说法中错误的是
- A.Se能形成SeO2、SeO3两种氧化物
- B.原子半径:Se>S
- C.H2Se比H2S稳定
- D.酸性:H2SeO4比H2SO4弱
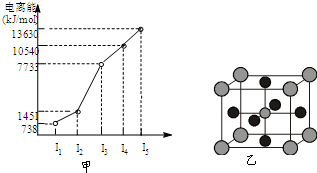 有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.
有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.请回答下列问题:
(1)X原子的电子排布式为
(2)第一电离能:X
(3)元素W的一种氢化物(化学式为W2H4)是重要的化工原料.有关W2H4分子的说法正确的是
A.分子中含有氢键 B.属于非极性分子
C.含有4个σ键和1个π键 D.W的原子与氢原子形成的化学键可以自由旋转
(4)X的氧化物与钛(Ti)的氧化物相互作用,能形成钛酸盐,其晶胞(晶体中最基本的重复单元)示意图如图乙所示.(X、Ti和O三种元素对应的离子分别位于立方体的体心、顶点和面心).该晶体中,钛离子和周围
(5)Z的气态氢化物分子中Z原子采用
A.离子键 B.非极性键C.配位键 D.极性键 E.金属键.
已知元素砷(As)的原子序数为33,下列叙述正确的是( )
| A、砷元素的最高化合价为+3 | B、砷元素是第四周期的主族元素 | C、砷原子的第3电子层含有16个电子 | D、砷的氧化物的水溶液呈弱碱性 |