网址:http://m.1010jiajiao.com/timu3_id_186020[举报]
实验室中有三瓶酸,分别是浓硫酸、浓盐酸和浓硝酸。
(1)写出三种酸中所有能够与铜发生反应的化学方程式。
_____________________________________________________________________________。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集气体1.12L(标准状况),则该气体的成分是 ,反应中所消耗的硝酸的物质的量可能为下列数据中的 。
A.0.1mol B.0.15mol C.0.2mol D.0.25mol
 (3)请设计一个实验装置,使铜与稀硫酸反应生成硫酸铜与氢气。在下面的方框内画出装置图,并标明电极材料名称和电解质溶液名称。
(3)请设计一个实验装置,使铜与稀硫酸反应生成硫酸铜与氢气。在下面的方框内画出装置图,并标明电极材料名称和电解质溶液名称。
(4) 实验室中欲用浓硫酸配制2.0mol·L-1的稀硫酸500mL。
①实验过程中所需仪器除了量筒、烧杯、玻璃棒外,还需要的仪器有________________________;
②下列操作中造成所配溶液浓度偏低的是_____________。
a.用量筒量取浓硫酸时仰视刻度线
b.定容时俯视刻度线
c.转移溶液后未洗涤烧杯和玻璃棒就直接定容
d.定容后摇匀,发现液面低于刻度,未补加蒸馏水至刻度
(5)下图所示为实验室模拟工业上利用氨催化氧化法制备硝酸的实验

用装置A制备干燥氨气,装置B制备干燥氧气。
①装置A的试管中发生反应的化学方程式为_____________________________________ 。
装置B的烧瓶内发生反应的化学方程式为______________________________________。
②下列关于A、B装置的叙述不正确的是__________
a.若选择合适的试剂用B装置也可制备氨气
b.实验过程中,A、B装置中一定有一个发生氧化还原反应
c.U形管中的试剂可以相同,但作用不相同
③按照a接c,b接d的顺序连接装置进行实验。
玻璃管内发生反应的化学方程式为_______________________________________。
查看习题详情和答案>>(16分)实验室由含铁废铜为原料生产胆矾(CuSO4·5H2O)和石膏(CaSO4·2H2O)的实验流程如图所示:
相关物质在不同温度下的溶解度(g/100g水)见下表。
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8[ | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是 (写化学式)。
(2)在进行操作I时的最佳温度是 ℃。
(3)从溶液中分离出产品II的操作II应为 、过滤、 、干燥。
(4)取样检验步骤中检验的是Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+。还可用KI来检验:2Fe3++2I-2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量FeCl3溶液和 (填少量、过量)的KI溶液。 | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至 (填仪器)中,倒入一定量的 , 。 |
|
| ③ |
|
|
查看习题详情和答案>>
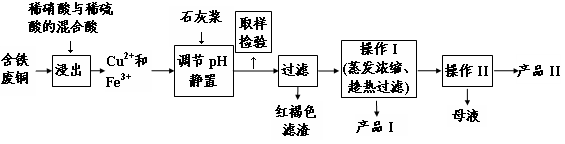
(16分)实验室由含铁废铜为原料生产胆矾(CuSO4·5H2O)和石膏(CaSO4·2H2O)的实验流程如图所示:
相关物质在不同温度下的溶解度(g/100g水)见下表。
|
温度(℃) |
20 |
40 |
60 |
80 |
100 |
|
石膏 |
0.32 |
0.26 |
0.15 |
0.11 |
0.07 |
|
胆矾 |
32 |
44.6 |
61.8[ |
83.8 |
114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是 (写化学式)。
(2)在进行操作I时的最佳温度是 ℃。
(3)从溶液中分离出产品II的操作II应为 、过滤、 、干燥。
(4)取样检验步骤中检验的是Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+。还可用KI来检验:2Fe3++2I- 2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
在试管中加入少量FeCl3溶液和 (填少量、过量)的KI溶液。 |
深红色如期出现 |
|
② |
将试管中的混合溶液转移至 (填仪器)中,倒入一定量的 , 。 |
|
|
③ |
|
|
查看习题详情和答案>>
(1)利用化学反应可以制备许多物质。实验室用铜制备NO2的离子方程式为_____________ ______。
(2)工业上,黄铜矿(主要成分CuFeS2)是提取铜的主要原料,可采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应:Cu2S+2Cu2O===6Cu+SO2↑。该反应中还原剂为_______ (填化学式),每生成1mol Cu,反应中转移电子的物质的量为___________。
黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。 ②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。 据以上信息回答下列问题:
a.通过上述②,炉渣中的Al2O3变成了 (写离子)。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 酸性KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
查看习题详情和答案>>
(1)利用化学反应可以制备许多物质。实验室用铜制备NO2的离子方程式为_____________ ______。
(2)工业上,黄铜矿(主要成分CuFeS2)是提取铜的主要原料,可采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应:Cu2S+2Cu2O===6Cu+SO2↑。该反应中还原剂为_______ (填化学式),每生成1mol Cu,反应中转移电子的物质的量为___________。
黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。 ②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。 据以上信息回答下列问题:
a.通过上述②,炉渣中的Al2O3变成了 (写离子)。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 酸性KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。