��Ŀ����
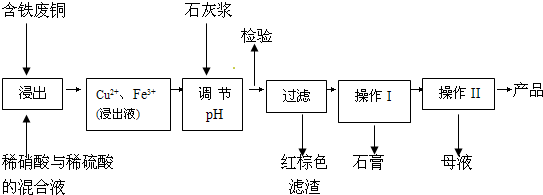
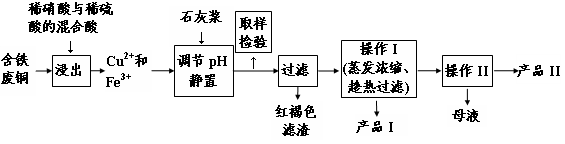
��16�֣�ʵ�����ɺ�����ͭΪԭ������������CuSO4��5H2O����ʯ�ࣨCaSO4��2H2O����ʵ��������ͼ��ʾ��
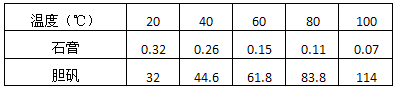
��������ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ�����±���
| �¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
| ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| ���� | 32 | 44.6 | 61.8[ | 83.8 | 114 |
��ش��������⣺
��1�����ɫ��������Ҫ�ɷ��� ��д��ѧʽ����
��2���ڽ��в���Iʱ������¶��� �档
��3������Һ�з������ƷII�IJ���IIӦΪ �����ˡ� �����
��4��ȡ�����鲽���м������Fe3+������Fe3+���������Լ��Ǵ����֪��KSCN�����Լ��������Fe3+��������KI�����飺2Fe3++2I��2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ���Թ��м�������FeCl3��Һ�� ������������������KI��Һ�� | ���ɫ���ڳ��� |
| �� | ���Թ��еĻ����Һת���� �����������У�����һ������ �� �� |
|
| �� |
|
|
��1��Fe(OH)3��2�֣� ��2��100��2�֣� ��3����ȴ�ᾧ ϴ�ӣ�2�֣�
��4����10�֣�
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ������2�֣� |
|
| �� | ��Һ©����1�֣���CCl4��1�֣�����ס�������������ȡ�������ã�1�֣� | Һ��ֲ㣬�ϲ�ӽ���ɫ���²��Ϻ�ɫ��1�֣� |
| �� | �������ȷų��²�Һ�壬�ٴӷ�Һ©�����Ͽ��е���ˮ�����Թ��У�����KSCN��Һ��2�֣� | ����Ѫ��ɫ����Ӧ��Ļ�����к�Fe3+������֤�����ȷ��һ�����淴Ӧ����֮��Fe3+������֤������һ�����淴Ӧ��2�֣� |
����:��1�������ĺ��ɫ����������������
��2�����������ڲ�ͬ�¶��µ��ܽ�ȿ�֪���������ܽ�����¶ȵ����߶�����ʯ����ܽ�����¶ȵ����߶����ͣ����Գ��ȹ��˵��¶�Ӧ��100��Ϊ�ˣ��������˵õ�����Ҫ��ʯ�ࡣ
��3�����ȹ��˵õ�����Һ���ȵ�����ͭ������Һ������ͨ����ȴ�ᾧ���õ�������Ȼ����ˣ�ϴ�ӣ����T�ɡ�
��4�����⻯�ز��㣬���Ȼ���һ����������˽��к����ķ�Ӧ�����Ե⻯��Ӧ�ǹ����ģ����ڹ���������£������ܼ���������ӣ����ע����Ӧ�ǿ��淴Ӧ����Ϊ��Ӧ���еⵥ�����ɣ�����Ϊ�˷�������ʵ⣬��Ҫͨ����ȡ����ȡ��Ҫ��Һ©������ȡ֮����ˮ��Һ�е���������KSCN��Һ�����������ӵĴ��ڼ��ɡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д���16�֣�ʵ�����ɺ�����ͭΪԭ������������CuSO4��5H2O����ʯ�ࣨCaSO4��2H2O����ʵ��������ͼ��ʾ��
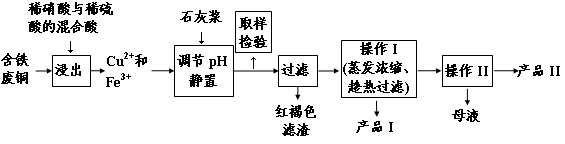
��������ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ�����±���
|
�¶ȣ��棩 |
20 |
40 |
60 |
80 |
100 |
|
ʯ�� |
0.32 |
0.26 |
0.15 |
0.11 |
0.07 |
|
���� |
32 |
44.6 |
61.8[ |
83.8 |
114 |
��ش��������⣺
��1�����ɫ��������Ҫ�ɷ��� ��д��ѧʽ����
��2���ڽ��в���Iʱ������¶��� �档
��3������Һ�з������ƷII�IJ���IIӦΪ �����ˡ� �����
��4��ȡ�����鲽���м������Fe3+������Fe3+���������Լ��Ǵ����֪��KSCN�����Լ��������Fe3+��������KI�����飺2Fe3++2I�� 2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
|
��� |
ʵ����� |
Ԥ������ͽ��� |
|
�� |
���Թ��м�������FeCl3��Һ�� ������������������KI��Һ�� |
���ɫ���ڳ��� |
|
�� |
���Թ��еĻ����Һת���� �����������У�����һ������ �� �� |
|
|
�� |
|
|
 2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
 2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ�� 