摘要:22.下图是探究浓.稀硝酸强氧化性的实验装置.将铜片置于具支试管的底部.在分液漏斗中加入约5mL 浓硝酸.用排水法收集产生的气体. Ⅰ.探究浓硝酸的强氧化性 打开分液漏斗活塞.向具支试管中注入约3mL浓硝酸. (1)具支试管中发生反应的化学方程式为 . (2)实验中能证明浓硝酸具有强氧化性的现象是 . . Ⅱ.探究稀硝酸的强氧化性 (3)欲证明稀硝酸也具有强氧化性.紧接着向分液漏斗中加适量水稀释浓硝酸.打开活塞.注入稀硝酸.这样操作的优点是 . (4)能证明稀硝酸与铜反应产生NO的实验现象是 . A.c中收集到无色气体, B.c中收集到的无色气体接触空气后变为红棕色, C.b中产生的无色气体接触空气后变为红棕色, Ⅲ.问题讨论 在实验过程中.研究性学习小组成员观察到铜和浓硝酸反应后溶液呈绿色.当加入稀硝酸反应后溶液呈蓝色.有人认为产生这一现象的原因是由于铜离子浓度差异所引起的.请你设计一个简单实验证明这一观点是错误的. .
网址:http://m.1010jiajiao.com/timu3_id_185515[举报]
某小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸.

可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,方程式:为2NO2+2NaOH=NaNO3+NaNO2+H2O.
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)组装仪器,检验气密性,通二氧化碳气体一段时间,关闭止水夹,将导管口伸进水槽中烧瓶里.通二氧化碳的目的是
(3)装置①中发生反应的化学方程式是
(4)装置②中发生反应的化学方程式是
(5)该小组得出结论所依据的实验现象是
查看习题详情和答案>>

可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,方程式:为2NO2+2NaOH=NaNO3+NaNO2+H2O.
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
3mol/L稀硝酸、浓硝酸、氢氧化钠溶液
3mol/L稀硝酸、浓硝酸、氢氧化钠溶液
.(2)组装仪器,检验气密性,通二氧化碳气体一段时间,关闭止水夹,将导管口伸进水槽中烧瓶里.通二氧化碳的目的是
排除装置中的氧气
排除装置中的氧气
.(3)装置①中发生反应的化学方程式是
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
.(4)装置②中发生反应的化学方程式是
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.(5)该小组得出结论所依据的实验现象是
④中液面上方气体变为红棕色,③中液面上方气体不变色
④中液面上方气体变为红棕色,③中液面上方气体不变色
.某小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸.
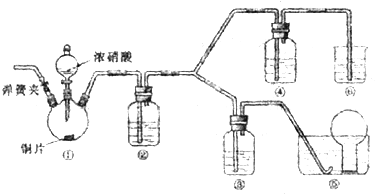
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,方程式:为2NO2+2NaOH=NaNO3+NaNO2+H2O.
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是______.
(2)组装仪器,检验气密性,通二氧化碳气体一段时间,关闭止水夹,将导管口伸进水槽中烧瓶里.通二氧化碳的目的是______.
(3)装置①中发生反应的化学方程式是______.
(4)装置②中发生反应的化学方程式是______.
(5)该小组得出结论所依据的实验现象是______.
查看习题详情和答案>>
某小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸.

可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,方程式:为2NO2+2NaOH=NaNO3+NaNO2+H2O.
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是______.
(2)组装仪器,检验气密性,通二氧化碳气体一段时间,关闭止水夹,将导管口伸进水槽中烧瓶里.通二氧化碳的目的是______.
(3)装置①中发生反应的化学方程式是______.
(4)装置②中发生反应的化学方程式是______.
(5)该小组得出结论所依据的实验现象是______.
查看习题详情和答案>>

可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,方程式:为2NO2+2NaOH=NaNO3+NaNO2+H2O.
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是______.
(2)组装仪器,检验气密性,通二氧化碳气体一段时间,关闭止水夹,将导管口伸进水槽中烧瓶里.通二氧化碳的目的是______.
(3)装置①中发生反应的化学方程式是______.
(4)装置②中发生反应的化学方程式是______.
(5)该小组得出结论所依据的实验现象是______.
查看习题详情和答案>>
某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)滴加浓硝酸之前先检验装置的气密性,再加入药品;打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(4)装置②的作用是
(5)该小组得出的结论依据的试验现象是
查看习题详情和答案>>

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
3mol/L稀硝酸、浓硝酸、氢氧化钠溶液;
3mol/L稀硝酸、浓硝酸、氢氧化钠溶液;
(2)滴加浓硝酸之前先检验装置的气密性,再加入药品;打开弹簧夹后
通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内
通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内
(3)装置①中发生反应的化学方程式是
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
(4)装置②的作用是
将NO2转化为NO
将NO2转化为NO
,发生反应的化学方程式是3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
(5)该小组得出的结论依据的试验现象是
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
.(14分)某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将![]() 氧化成
氧化成![]() ,而稀硝酸不能氧化
,而稀硝酸不能氧化![]() 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。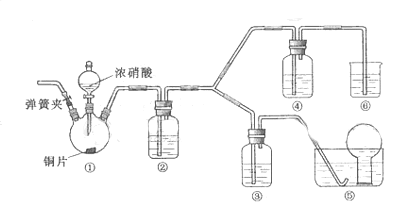
![]()
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与![]() 反应,能与
反应,能与![]() 反应
反应
![]()
(1) 实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
(2) 滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3) 装置①中发生反应的化学方程式是
(4) 装置②的作用是 ,发生反应的化学方程式是
(5) ![]() 该小组得出的结论一局的试验现象是
该小组得出的结论一局的试验现象是
(6) ![]() 试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
a. ![]() 加热该绿色溶液,观察颜色变化
加热该绿色溶液,观察颜色变化
b. ![]() 加水稀释绿色溶液,观察颜色变化
加水稀释绿色溶液,观察颜色变化
c. ![]() 向该绿色溶液中通入氮气,观察颜色变化
向该绿色溶液中通入氮气,观察颜色变化
d. ![]() 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
查看习题详情和答案>>