摘要:1.下列化合物在自然界能稳定存在的是 A.Na2O B.NaI C.NaClO D.NaCl
网址:http://m.1010jiajiao.com/timu3_id_184795[举报]
元素在元素周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分:
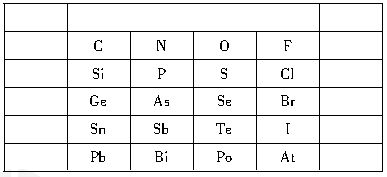
(1)一般地,同一主族的元素最外层电子数相同,其单质及其对应的化合物具有相似的性质。下列对同主族元素所组成的物质的性质的推理中不正确的是______。
A.Na与Cl2反应能形成离子键,故K与Cl2反应也能形成离子键
B.Cl2能置换出NaBr溶液中的溴,故Br2也能置换出KI溶液中的碘
C.Li在氧气中燃烧生成Li2O,故Na在氧气中燃烧生成Na2O
D.C在自然界有稳定的单质存在,故Si在自然界也有稳定的单质存在
(2)表中P元素原子的电子排布式为_________;As的原子结构示意图是__________________。
(3)根据元素周期律,请你预测:
H3AsO4、H3PO4的酸性强弱:________>_______;As、Se气态氢化物的稳定性:________>________。
(4)比较N和O的第一电离能的大小:________>______,原因是______________________________。 查看习题详情和答案>>

(1)一般地,同一主族的元素最外层电子数相同,其单质及其对应的化合物具有相似的性质。下列对同主族元素所组成的物质的性质的推理中不正确的是______。
A.Na与Cl2反应能形成离子键,故K与Cl2反应也能形成离子键
B.Cl2能置换出NaBr溶液中的溴,故Br2也能置换出KI溶液中的碘
C.Li在氧气中燃烧生成Li2O,故Na在氧气中燃烧生成Na2O
D.C在自然界有稳定的单质存在,故Si在自然界也有稳定的单质存在
(2)表中P元素原子的电子排布式为_________;As的原子结构示意图是__________________。
(3)根据元素周期律,请你预测:
H3AsO4、H3PO4的酸性强弱:________>_______;As、Se气态氢化物的稳定性:________>________。
(4)比较N和O的第一电离能的大小:________>______,原因是______________________________。 查看习题详情和答案>>
一般来说,同一主族的元素最外层电子数相同,其单质及其对应的化合物具有相似的性质。下列关于同主族元素所形成的物质的性质推理中,正确的是
[ ]
A.Li在氧气中燃烧生成Li2O,故Na在氧气中燃烧也生成Na20
B.Cl2能置换出NaBr溶液中的溴,故I2也能置换出NaBr溶液中的溴
C.Na与Cl2反应能形成离子键,故K与Cl2反应也能形成离子键
D.C在自然界有稳定的单质存在,故Si在自然界也有稳定的单质存在
查看习题详情和答案>>
B.Cl2能置换出NaBr溶液中的溴,故I2也能置换出NaBr溶液中的溴
C.Na与Cl2反应能形成离子键,故K与Cl2反应也能形成离子键
D.C在自然界有稳定的单质存在,故Si在自然界也有稳定的单质存在
现有部分元素的原子结构特点如表:
(1)画出W原子结构示意图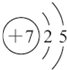
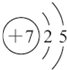 .
.
(2)元素X与元素Z相比,非金属性较强的是
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
查看习题详情和答案>>
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 最外层电子数是次外层电子数的2.5倍 |
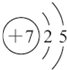
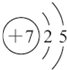
(2)元素X与元素Z相比,非金属性较强的是
X(或氧)
X(或氧)
,写出一个能表示X、Z非金属性强弱关系的化学反应方程式S+O2
SO2或2H2S+O2═2H2O+2S
| ||
S+O2
SO2或2H2S+O2═2H2O+2S
.
| ||
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
NH4HSO4
NH4HSO4
.(4)元素X和元素Y以原子个数比1:1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等.以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
N2H4+2H2O2
N2+4H2O
| ||
N2H4+2H2O2
N2+4H2O
.
| ||
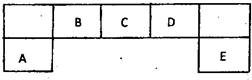 短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素形成的化合物在自然界中的种类最多.请回答下列问题
短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素形成的化合物在自然界中的种类最多.请回答下列问题(1)描述D在元素周期表中的位置:
第二周期第ⅥA族
第二周期第ⅥA族
(2)比较A、C、D元素简单离子半径的大小:
N3-
N3-
>O2-
O2-
>Al3+
Al3+
(填微粒符号)(3)F与D同主族且相邻,请说出D的氢化物比F的氢化物稳定的根本原因:
N的非金属性比S强
N的非金属性比S强
(4)C的氢化物与其最高价氧化物对应的水化物反应,产物溶于水呈
酸
酸
性,用离子方程式解释原因NH4++H2O?NH3.H2O+H+
NH4++H2O?NH3.H2O+H+
.(5)D原子与氢原子可形成10电子阳离子,写出该阳离子的电子式


(6)E的最高价氧化物的水化物的化学式为
HClO4
HClO4
.E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,该反应的化学反应方程式为8HCl+KClO4
KCl+4Cl2↑+4H2O
| ||
8HCl+KClO4
KCl+4Cl2↑+4H2O
.
| ||