网址:http://m.1010jiajiao.com/timu3_id_183480[举报]
镁在空气中燃烧除生成MgO外,还可能生成Mg3N2 。某校化学兴趣小组的同学利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成。
(1)甲组同学取一定量燃烧后的固体投入水中,得到了一种能使湿润的红色石蕊试纸变蓝 的气体,该气体的化学式为 ,说明固体中含有Mg3N2,生成该气体的化学反应方程式为 。
(2)乙组同学为测定Mg3N2含量,用图示装置进行实验,充分反应后再加热A。其中浓硫酸的作用是 ,对A加热的目的是 。已知加入的固体质量为4.0g,最终C装置增重ag,则固体中含Mg3N2 g(用含a的式子表示)。

(3)丙组有的同学认为乙组同学的测定结果偏高,理由是
。
有的同学认为乙组同学的测定结果偏低,理由是
。
丙组同学进行了改进,他们将乙组同学实验中得到的难溶固体进行过滤、洗涤、干燥,并
灼烧固体至恒重,测得其质量为4.08g。上述过程中,洗涤沉淀的操作是
。
镁在空气中燃烧后生成的固体中Mg3N2的质量分数为 。
有一种用铵盐与含镁矿石混合煅烧制取氧化镁的方法,解决了现有方法存在的原料成 本高、项目投资大、能耗高、副产品不好用等问题,其原理是将含镁矿石粉(含氧化镁)与 铵盐混合,经过煅烧、水溶、过滤,得到粗镁盐溶液,并回收煅烧产生的氨。写出用固体(NH4)2SO4与含镁矿石粉煅烧的化学反应方程式
。
查看习题详情和答案>>|
某种单质硫的化学式为S8,S8在足量的氧气中完全燃烧生成SO2,如果S8的物质的量为n1 mol,生成的SO2的物质的量为n2 mol,则n1n2的关系是 | |
| [ ] | |
A. |
8n1=n2 |
B. |
n1=8n2 |
C. |
n1=n2 |
D. |
不能确定 |
甲、乙两同学分别设计了如图所示的两套实验装置(所取的铁粉均为a g):

请回答下列问题:
(一)装置的评价
(1)在水蒸气的生成装置中乙同学在烧瓶底部放置了几片碎瓷片,其作用是___________;
(2)在反应装置中甲同学在硬质玻璃管中放入的是还原铁粉和石棉绒,石棉绒的作用是___
__________________;
(3)在收集装置中甲同学用的是排水集气法,这种方法存在的安全隐患是___________。
(二)实验过程
(4)甲同学可以证明两者发生反应的现象是______________________;
(5)从反应物元素的种类分析,生成的气体可能是氢气,进一步验证的方法是_________;
(6)当玻璃管中的铁粉充分反应后,停止实验,称量反应后固体产物质量为b,则固体产物的化学式为___________(用字母表示)。
(三)问题讨论
(7)酒精灯和酒精喷灯点燃的顺序是_____________。
(8)为了防止甲中气体收集装置发生的安全问题,可以在不增减仪器种类、数量,不改变其连接方式的前提下进行简单的改造,请在甲中画出你改造之处的示意图。
查看习题详情和答案>>(1)合成氨反应N2(g)+3H2(g)
 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。(2)一氧化碳在高温下与水蒸气反应的方程式为:CO+H2O=CO2+H2。已知部分物质燃烧的热化学方程式如下: 2H2(g) + O2(g)= 2H2O(l);△H=-571.6kJ·mol-1
2CO (g) + O2(g)= 2CO2 (g) ;△H=-566kJ·mol-1
又知1molH2O(g)转变为1mol H2O(l)时放出44.0kJ热量。写出CO和水蒸气在高温催化剂下反应的热化学方程式 。
(3)在25℃下,向浓度均为0.1 mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学
 式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl—NH4Cl为电解质溶液制造新型燃烧电池,放电过程中,溶液中铵根离子浓度逐渐增大。请写出该电池的正极反应式 。
(5)某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11。在此温度下,将pH=1的H2SO4溶液VaL与pH=11的NaOH溶液VbL混合,若所得混合液为
 中性,则Va︰Vb= 。
中性,则Va︰Vb= 。(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-)。则溶液显_____________性(填“酸”“碱”或“中”);
(7)NH4Cl是一种重要的化肥。
①用0.1 mol·L—1的盐酸滴定0.1 mol·L—1的氨水,滴定过程中不可能出现的结果是:
a.

b.

c.
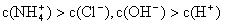
d.

②NH4Cl溶液中存在:NH4+ + H2O
 NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)
NH3·H2O + H+,则该反应常温下的平衡常数K= (已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10—5 mol·L—1)