摘要: 下表中属于同一种元素的一组原子是 原子种类 甲 乙 丙 丁 戊 质子数 6 6 6 8 9 中子数 6 7 8 8 8 A. 甲.乙和丙 B.丙.丁和戊 C. 甲.丙和丁 D.乙.丙和戊 答案:1.B 2.A.
网址:http://m.1010jiajiao.com/timu3_id_18046[举报]
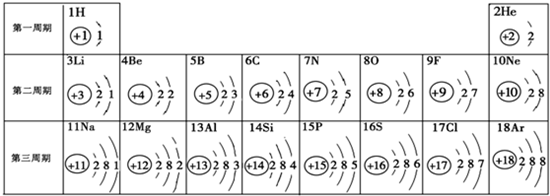
元素周期表是化学学习和研究的重要工具.下图是元素周期表的一部分.

(1)从表中查出硅(Si)元素的相对原子质量为
(2)锂元素和氢元素
(3)表中不同种元素最本质的区别是
A.质子数不同 B.中子数不同 C.相对原子质量不同
(4)由l、7、8号元素组成的一种物质的化学式为
查看习题详情和答案>>

(1)从表中查出硅(Si)元素的相对原子质量为
28.09
28.09
;(2)锂元素和氢元素
不是
不是
(选填“是”或“不是”)属于同一周期的元素;(3)表中不同种元素最本质的区别是
A
A
(填序号):A.质子数不同 B.中子数不同 C.相对原子质量不同
(4)由l、7、8号元素组成的一种物质的化学式为
HNO3或NH4NO3
HNO3或NH4NO3
.元素周期表是学习和研究化学的重要工具.请据表(元素周期表的部分内容)回答有关问题:
(1)请从表中查出关于硼元素的一条信息:
(2)第3周期(横行)中属于金属元素的是
(3)第11号元素与第17号元素组成的化合物化学式是
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl.
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
硼元素的原子序数为5等
硼元素的原子序数为5等
;(2)第3周期(横行)中属于金属元素的是
钠
钠
(填一种),其阳离子是Na+(合理即可)
Na+(合理即可)
;(3)第11号元素与第17号元素组成的化合物化学式是
NaCl
NaCl
,构成该物质的微粒是离子
离子
(选填“分子”、原子”或“离子”);(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质.则下列各组元素具有相似化学性质的是
bd
bd
(填标号).a.C和Ne b.Be和Mg c.Al和Si d.F和Cl.
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题:
(1)在元素周期表中,原子序数为12的元素符号是 ,在化学反应中该原子易
,在化学反应中该原子易
(2)写出原子序数为1、8、11三种元素所组成化合物的化学式
(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,最外层电子数依次增加;
③
查看习题详情和答案>>
| 第一周期 | 1 H 氢 |
2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
| 第三周期 | 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
Mg
Mg
,其原子结构示意图为 ,在化学反应中该原子易
,在化学反应中该原子易失去
失去
(填“得到”或“失去”)电子.13号元素属于金属
金属
(填“金属”或“非金属”)元素.(2)写出原子序数为1、8、11三种元素所组成化合物的化学式
NaOH
NaOH
.写出12号元素与17号元素形成化合物的化学式为MgCl2
MgCl2
.(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,最外层电子数依次增加;
③
同一横行的原子,电子层数相同
同一横行的原子,电子层数相同
(任写一条).
 ,该元素的原子核外有
,该元素的原子核外有