题目内容
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题:
(1)在元素周期表中,原子序数为12的元素符号是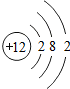 ,在化学反应中该原子易
,在化学反应中该原子易
(2)写出原子序数为1、8、11三种元素所组成化合物的化学式
(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,最外层电子数依次增加;
③
| 第一周期 | 1 H 氢 |
2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
| 第三周期 | 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
Mg
Mg
,其原子结构示意图为 ,在化学反应中该原子易
,在化学反应中该原子易失去
失去
(填“得到”或“失去”)电子.13号元素属于金属
金属
(填“金属”或“非金属”)元素.(2)写出原子序数为1、8、11三种元素所组成化合物的化学式
NaOH
NaOH
.写出12号元素与17号元素形成化合物的化学式为MgCl2
MgCl2
.(3)通过分析,同一横行元素之间的排列有一定的规律,例如:
①从左到右,由金属元素逐渐向非金属元素过渡;
②从左到右,最外层电子数依次增加;
③
同一横行的原子,电子层数相同
同一横行的原子,电子层数相同
(任写一条).分析:(1)依据元素周期表中的各部分的信息以及原子结构示意图的有关特点分析解答;
(2)依据原子序数判断该元素的种类,而后依据相关元素的化合价情况书写化学式即可;
(3)依据同一周期的元素的共同点分析解答;
(2)依据原子序数判断该元素的种类,而后依据相关元素的化合价情况书写化学式即可;
(3)依据同一周期的元素的共同点分析解答;
解答:解:(1)依据12号元素在表中的信息可知该元素的符号为Mg,由于镁原子的最外层电子数是2,化学反应中失去最外层的两个电子,从而达到稳定结构,13号元素是铝元素,其名称中含有“钅”旁,所以属于金属元素;
(2)原子序数为1、8、11三种元素分别是氢、氧和钠,所以三者组成的化合物化学式为NaOH,12号元素与17号元素分别是镁与氯元素,所以两者形成的化合物化学式为MgCl2;
(3)同一横行元素之间的排列有一定的规律除①②外还可以有同一横行的电子层数相同等共同点;
故答案为:(1)Mg;失去;金属;(2)NaOH;MgCl2;(3)同一横行的原子,电子层数相同;
(2)原子序数为1、8、11三种元素分别是氢、氧和钠,所以三者组成的化合物化学式为NaOH,12号元素与17号元素分别是镁与氯元素,所以两者形成的化合物化学式为MgCl2;
(3)同一横行元素之间的排列有一定的规律除①②外还可以有同一横行的电子层数相同等共同点;
故答案为:(1)Mg;失去;金属;(2)NaOH;MgCl2;(3)同一横行的原子,电子层数相同;
点评:本题考查学生熟练掌握应用元素周期表所提供的信息进行分析解题的能力,难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
化学是研究物质的,而物质是由肉眼看不到的分子、原子和离子等微观粒子构成的,让我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界.
(1)金秋十月,丹桂飘香,我能从分子的角度分析其原因是 .
(2)下图是某反应的微观示意图,依据此图回答下列问题: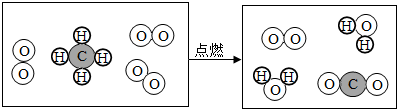
反应物中化合物的化学式为 ,生成物中各物质的粒子个数比是 ,从微观的角度还能获得一条关于物质变化的信息是 .
(3)元素周期表是我们学习化学的重要工具.下表是小丽同学绘制的元素周期表的局部,依据此表回答问题:
①我发现其中有一处元素符号不正确,应该改为 ;
②地壳中含量最多的元素原子的质子数是 ,在化学反应中它易 (填“得到”或“失去”)电子.
③磷元素在元素周期表中位于第 周期.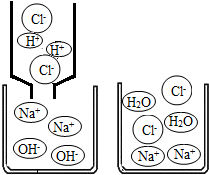
(4)右图是两种溶液恰好完全反应的微观示意图,我能写出此反应的化学方程式 ,反应后所得溶液中含有的粒子有(填符号) .
(1)金秋十月,丹桂飘香,我能从分子的角度分析其原因是
(2)下图是某反应的微观示意图,依据此图回答下列问题:

反应物中化合物的化学式为
(3)元素周期表是我们学习化学的重要工具.下表是小丽同学绘制的元素周期表的局部,依据此表回答问题:
| 1 H 氢 |
2 氦 | ||||||
| 3 锂 |
4 铍 |
5 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 氖 |
| 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 SI 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 氩 |
②地壳中含量最多的元素原子的质子数是
③磷元素在元素周期表中位于第

(4)右图是两种溶液恰好完全反应的微观示意图,我能写出此反应的化学方程式

 在化学反应中该原子
在化学反应中该原子
 在化学反
在化学反