网址:http://m.1010jiajiao.com/timu3_id_180452[举报]
用单质硫与金属单质R在加热条件下可生成化合物M,如把![]() 溶液加入到R的硫酸盐溶液中,也可得到不溶性物质M,则R和M可能是
溶液加入到R的硫酸盐溶液中,也可得到不溶性物质M,则R和M可能是
[
]A
.Na、 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:(1)元素的非金属性为(原子的得电子能力):Q
(2)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
| ||
| ||
(3)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ.又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H=
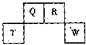 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:(1)T的离子结构示意图为


(2)元素的非金属性为(原子的得电子能力):Q
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
| ||
| ||
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
| ||
| ||
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
I、磷、硫元素的单质和化合物应用广泛.
(1)磷元素的原子核外电子排布式是
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2→6CaSiO3+P4O10 10C+P4O10→P4+10CO
每生成1mol P4时,就有
II、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
(1)铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3?6H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是
(2)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:
在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L.
反应物A的浓度随时间的变化如图所示.
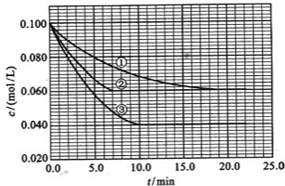
请回答下列问题:
(3)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是:②
③
(4)实验②平衡时B的转化率为
(5)该反应是
(6)该反应进行到4.0min时的平均反应速度率:
实验②:VB=
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

1.T的离子结构示意图为________.
2.元素的非金属性为(原子的得电子能力):Q________W(填“强于”或“弱于”).
3.W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为________.
4.原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________.
5.R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是________.
Ⅰ、磷、硫元素的单质和化合物应用广泛.
6.磷元素的原子核外电子排布式是________.
7.磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2→6CaSiO3+P4O10 10C+P4O10→P4+10CO
每生成1 mol P4时,就有________mol电子发生转移.
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
8.铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是________.
9.在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:
________Ce3++________H2O2+________H2O→________Ce(OH)4↓+________.