题目内容
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

1.T的离子结构示意图为________.
2.元素的非金属性为(原子的得电子能力):Q________W(填“强于”或“弱于”).
3.W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为________.
4.原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________.
5.R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是________.
Ⅰ、磷、硫元素的单质和化合物应用广泛.
6.磷元素的原子核外电子排布式是________.
7.磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2→6CaSiO3+P4O10 10C+P4O10→P4+10CO
每生成1 mol P4时,就有________mol电子发生转移.
Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
8.铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是________.
9.在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:
________Ce3++________H2O2+________H2O→________Ce(OH)4↓+________.
解析:
1.(1分)![]()
2.(1分)弱于
3.(2分)S+2H2SO4(浓)![]() 3SO2↑+2H2O
3SO2↑+2H2O
4.(2分)2H2O2![]() 2H2O+O2↑(或其他合理答案:)
2H2O+O2↑(或其他合理答案:)
5.(2分)NaNO2
6.(2分)1s22s22p63s23p3;
7.(2分)20;
8.(2分)分解出HCl气体,抑制CeCl3的水解(或其他合理答案);
9.(2分)2Ce3++H2O2+6H2O→2Ce(OH)4↓+6H+

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案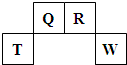 (2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
(2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:
 (2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )
(2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )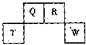 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: