网址:http://m.1010jiajiao.com/timu3_id_175689[举报]
 游泳池中的水经常要消毒杀菌.某化学兴趣小组对游泳池中使用的消毒剂进行了研究性学习.
游泳池中的水经常要消毒杀菌.某化学兴趣小组对游泳池中使用的消毒剂进行了研究性学习.(1)氯气是游泳池中水体消毒杀菌的常用消毒剂之一,它能消毒杀菌的原因是(用离子方程式表示)
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5mg/L至1.0mg/L之间时,效果最好.右图是该组测定某星期中每天19:00时游泳池中水的氯含量.根据图示判断,哪几天的天气炎热、阳光强烈,并说明理由
(3)游泳池也可使用漂白液(主要成份是NaClO)来进行消毒杀菌.与氯气相比较,请写出使用漂白液的优点之一
(4)广谱消毒剂ClO2已被世界卫生组织(WHO)列为A1级高效安全灭菌消毒剂.若消毒同一游泳池中的水,达到同样的消毒效果,所需ClO2与Cl2的物质的量之比为
(5)用于游泳池消毒杀菌的消毒剂还有很多.下列物质中,也可以用于游泳池杀菌消毒的有
A、二氧化硫 B、臭氧 C、活性炭 D、高锰酸钾.
I.关于反应物之间的定量关系的研究:
(1)已知反应:2I-+2Fe3+=I2+2Fe2+,向100mL,0.1moL?L-1的FeI2溶液中通入0.01mol Cl2,该反应的离子方程式为
(2)298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,将物质的量浓度均为2×10-4mol?L-1的氯化镁溶液和氢氧化钠溶液等体积混合,能否产生氢氧化镁沉淀?
Ⅱ,关于反应速率、限度的研究:
近段时间,全国范围内的雾霾天气严重影响了人们的身体健康.环境问题越来越受到人们的重视.汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒.以CO为例,其中毒原理是相同温度下CO与血红蛋白的结合能力远远大于氧气与血红蛋白的结合能力,反应如下:CO+HbO2?O2+HbCO(HbO2表示氧合血红蛋白).
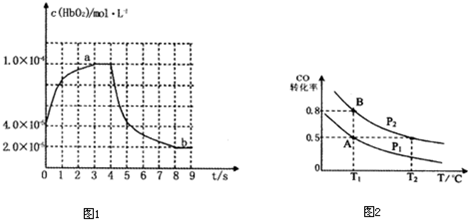
如图表示HbO2浓度随时间的变化:曲线a表示向血样中通入氧气后的变化;曲线b表示在第4s时通入CO和O2混合气体后的变化.
(3)前3s以HbO2表示的平均反应速率为
(4)37℃时,CO+HbO2?O2+HbCO,该反应的平衡常数K=220,资料显示HbCO的浓度达到HbO2浓度的0.022倍,就会导致人体智力受损.据此,通过计算可知,当吸入的CO与O2浓度之比大于或等于
| 1 |
| 10000 |
| 1 |
| 10000 |
(5)一氧化碳、氢气既是重要的能源,也可以催化还原NO等消除污染,还可以在一定条件下制取CH3OH.已知
N2(g)+O2(g)=2NO((g)△H=+180.5kJ?mol-1
2H2(g)+O2(g)=2H2O(1)△H=-571.6kJ?mol-1
H2O(g)=H2O(1)△H=-44kJ?mol-1
写出H2与NO反应生成N2和水蒸气的热化学方程式
(6)在一容积可变的密闭容器中充入10mol CO和20molH2,在催化剂存在时反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率随温度(T)、压强(P)的变化如右图所示,当达到平衡状态A时,容器的体积为10L.如反应开始时仍充入10mol CO和20mol H2,则在平衡状态B时容器的体积V(B)=
测定某有机化合物甲的结构,进行如下实验:
[分子式的确定]
(1)经测定有机物甲由C、H、O三种元素组成,元素的质量比为12∶3∶8,其蒸气密度是H2密度的23倍.根据价键理论,预测甲的可能结构并写出结构简式________.
[结构式的确定]
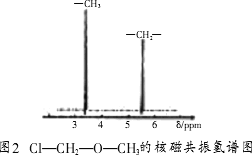
(2)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(图2).经测定,有机物甲的核磁共振氢谱示意图如图3,则甲的结构简式为________.
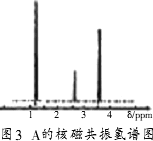
[性质探究]将温度控制在400℃以下,根据图4,按要求完成实验.(已知甲的沸点为78.5℃)
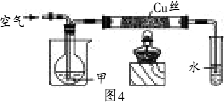
(3)在通入空气的条件下进行实验Ⅰ.
甲的名称是________,加入药品后的操作依次是________.
a.打开活塞
b.用鼓气球不断鼓入空气
c.点燃酒精灯给铜丝加热
(4)在停止通入空气的条件下进行实验Ⅱ.
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是________;
②甲蒸气进入反应管后,在铜作催化剂及
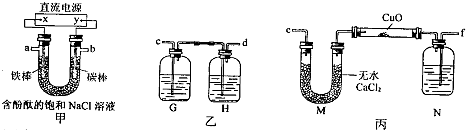
(1)直流电源中的X极为
(2)为完成上述实验,正确的链接顺序为:a连
(3)装置乙中的G瓶内溶液可能为
A.淀粉KI溶液B.NaOH溶液C.Na2S溶液D.Na2SO3溶液
H瓶内的反应的离子方程式为:
(4)在对硬质玻璃试管里的氧化铜粉末加热前需要进行的操作为:
(5)装置丙中N瓶内盛放的试剂为
(6)为了测定Cu的相对原子质量,某同学通过实验测得如一下数据:
I.氧化铜样品质量为m1g
Ⅱ.反应后硬质玻璃管中剩余固体质量为m2g
III.反应前后U形管及其固体质量差为m3g
Ⅳ.反应前后瓶及其液体质量差为m4g
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)=
②如果选用其它数据进行计算,会导致Ar(Cu)
某化学兴趣小组拟采用下图所示装置电解饱和氯化钠溶液制备H2,通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),同时检验Cl2的氧化性(图中夹持和加热仪器已略去)。
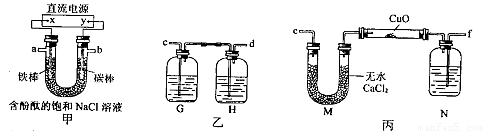
(1)直流电源中的X极为 极(填“正”、“负”、“阴”或“阳”);写出甲装置U形管中反应的离子方程式: ;实验开始后,用铁棒作电极的一侧的实验现象是 。
(2)为完成上述实验,正确的链接顺序为:a连 ,b连 (填写连接的字母)。
(3)装置乙中的G瓶内溶液可能为 (填字母)。
A.淀粉KI溶液 B.NaOH溶液 C.Na2S溶液 D.Na2SO3溶液
H瓶内的反应的离子方程式为: 。
(4)在对硬质玻璃试管里的氧化铜粉末加热前需要进行的操作为: 。
(5)装置丙中N瓶内盛放的试剂为 ,作用是 。
(6)为了测定Cu的相对原子质量,某同学通过实验测得如一下数据:
I.氧化铜样品质量为m1g
Ⅱ.反应后硬质玻璃管中剩余固体质量为m2g
Ⅲ.反应前后U形管及其固体质量差为m3g
Ⅳ.反应前后瓶及其液体质量差为m4g
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)= 。
②如果选用其它数据进行计算,会导致Ar(Cu) (填“偏大”、“偏小”或“无影响”),理由是 。
查看习题详情和答案>>