摘要:19.下图中.A.B.C.D.E含有同一元素.A为红棕色固体.B为黑色粉末.C的溶液呈黄色.D的溶液呈浅绿色.E为白色沉淀且在空气中迅速转变为灰绿色最终变为红褐色.X是一种酸性稀溶液.Y是一种碱性稀溶液.其他生成物均已略去. 填写下列空白: ⑴A的化学式是 .X的化学式是 . ⑵反应④的离子方程式是 .该反应中的氧化剂是 .
网址:http://m.1010jiajiao.com/timu3_id_171682[举报]
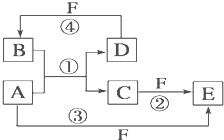 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).(1)若A为短周期金属单质,D为短周期非金属单质(一种黑色固体),且所含元素的原子序数A是D的2倍,原子的最外层电子数D是A的2倍,化合物F的浓溶液与单质A、D在一定条件下反应都有红棕色气体生成,则A在周期表中的位置为:
第三周期,ⅡA族
第三周期,ⅡA族
,B的电子式为::O::C::O:
:O::C::O:
,F的浓溶液与D在加热条件下反应的化学方程式为:C+4HNO3
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3
CO2↑+4NO2↑+2H2O
.
| ||
(2)若A是常见变价金属的单质,D、F是气态单质,且反应①②均在水溶液中进行.则反应②的离子方程式是
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(3)若A、D、F都是短周期非金属元素单质,且 A、D所含元素同主族,A、F所含元素同周期,B是制作光导纤维的基本原料,则B是
SiO2
SiO2
,C是CO
CO
,F是O2
O2
.(填化学式) A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D在常温下都是气体,B为红棕色.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D在常温下都是气体,B为红棕色.(1)写出各下列物质的化学式:则A是
N2
N2
,D是NH3
NH3
;(2)写出下列反应的化学方程式:B→C
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
,E→C8HNO3+3Cu=3Cu(NO3)2+2NO+4H2O
8HNO3+3Cu=3Cu(NO3)2+2NO+4H2O
.A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸.请根据以上信息回答下列问题.
(1)B元素在元素周期表中的位置是第
(2)画出D元素的原子结构示意图
 .
.
(3)与E的氢化物分子所含电子总数相等的分子是
(4)A与C形成的化合物中含有化学键的类型是
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
查看习题详情和答案>>
(1)B元素在元素周期表中的位置是第
三
三
周期IA
IA
族.(2)画出D元素的原子结构示意图


(3)与E的氢化物分子所含电子总数相等的分子是
H2O
H2O
(举一例、填化学式,下同)、离子是OH-
OH-
.(4)A与C形成的化合物中含有化学键的类型是
共价键
共价键
.(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
Cl2+2OH-=ClO-+Cl-+H2O
Cl2+2OH-=ClO-+Cl-+H2O
.A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.其中B的单质在常温下为双原子分子,它与A的单质可形成气态分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期元素中原子半径最大的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子.则
(1)B的原子结构示意图为
 ;X的化学名称为
;X的化学名称为
(2)B单质的结构式为
(3)B、C、E分别与A形成的化合物中最稳定的是
(4)D是同周期简单阳离子中离子半径最
(5)F的单质在反应中常作
查看习题详情和答案>>
(1)B的原子结构示意图为


氨气
氨气
.(2)B单质的结构式为
N≡N
N≡N
;E的气态氢化物的结构式为H-S-H
H-S-H
;C与D形成的两种化合物中,其中一种物质含有两种类型的化学键,分别为离子键、共价键
离子键、共价键
,该物质属于离子化合物
离子化合物
(填“离子化合物”或“共价化合物”).(3)B、C、E分别与A形成的化合物中最稳定的是
H2O
H2O
(写化学式).(4)D是同周期简单阳离子中离子半径最
大
大
的元素.(5)F的单质在反应中常作
氧化
氧化
剂(填“氧化”或“还原”). A、B、C、D、E五种中学常见物质均含有同一种元素,且A为单质,有如图所示的转化关系.则下列分析中不正确的是( )
A、B、C、D、E五种中学常见物质均含有同一种元素,且A为单质,有如图所示的转化关系.则下列分析中不正确的是( )