题目内容
A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的-1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸.请根据以上信息回答下列问题.
(1)B元素在元素周期表中的位置是第
(2)画出D元素的原子结构示意图
 .
.
(3)与E的氢化物分子所含电子总数相等的分子是
(4)A与C形成的化合物中含有化学键的类型是
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
(1)B元素在元素周期表中的位置是第
三
三
周期IA
IA
族.(2)画出D元素的原子结构示意图


(3)与E的氢化物分子所含电子总数相等的分子是
H2O
H2O
(举一例、填化学式,下同)、离子是OH-
OH-
.(4)A与C形成的化合物中含有化学键的类型是
共价键
共价键
.(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式为
Cl2+2OH-=ClO-+Cl-+H2O
Cl2+2OH-=ClO-+Cl-+H2O
.分析:(1)根据元素的离子结构来确定元素,进而确定所在的位置;
(2)根据元素的离子结构来确定元素并画原子结构示意图;
(3)根据10电子微粒知识来回答;
(4)非金属原子间形成的化学键大多是共价键;
(5)氯气能和强碱反应生成氯化物、次氯酸盐和水.
(2)根据元素的离子结构来确定元素并画原子结构示意图;
(3)根据10电子微粒知识来回答;
(4)非金属原子间形成的化学键大多是共价键;
(5)氯气能和强碱反应生成氯化物、次氯酸盐和水.
解答:解:(1)B的+1价阳离子与氖原子具有相同的电子层结构,所以B是金属Na,在第三周期第ⅠA族,故答案为:三;ⅠA;
(2)C的-1价阴离子都与氖原子具有相同的电子层结构,所以C是F,D在F的下一周期,可与Na形成BD型离子化合物,即为氯化钠,D为Cl,原子结构示意图为: ,
,
故答案为: ;
;
(3)E和F为同一周期元素,其最高价氧化物对应的水化物为一种强酸即为硝酸,所以E是N,E的氢化物是氨气,10电子结构,所含电子总数相等的分子有H2O、CH4、HF等,离子有Na+、O2-、OH-、Mg2+、Al3+等,故答案为:H2O(CH4、HF);OH-(Mg2+、Al3+、Na+、O2-);
(4)A是相对原子质量最小的元素即为H,H和F形成的是含有共价键的共价化合物,故答案为:共价键;
(5)氯气和氢氧化钠反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O,故答案为:Cl2+2OH-=ClO-+Cl-+H2O.
(2)C的-1价阴离子都与氖原子具有相同的电子层结构,所以C是F,D在F的下一周期,可与Na形成BD型离子化合物,即为氯化钠,D为Cl,原子结构示意图为:
 ,
,故答案为:
 ;
;(3)E和F为同一周期元素,其最高价氧化物对应的水化物为一种强酸即为硝酸,所以E是N,E的氢化物是氨气,10电子结构,所含电子总数相等的分子有H2O、CH4、HF等,离子有Na+、O2-、OH-、Mg2+、Al3+等,故答案为:H2O(CH4、HF);OH-(Mg2+、Al3+、Na+、O2-);
(4)A是相对原子质量最小的元素即为H,H和F形成的是含有共价键的共价化合物,故答案为:共价键;
(5)氯气和氢氧化钠反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O,故答案为:Cl2+2OH-=ClO-+Cl-+H2O.
点评:本题考查学生元素周期律和元素周期表的综合知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
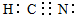
 CH3COOH+OH-
CH3COOH+OH- 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示) 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是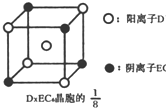
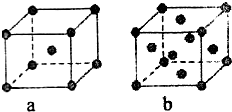 已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.
已知A、B、C、D、E都是元素周期表中的前四周期元素,它们原子序数的大小关系为A<C<B<D<E.又知A原子的p轨道为半充满,其形成的氢化物的沸点是同主族非金属元素的氢化物中最高的.D原子得到一个电子后其3p轨道将全充满.B+离子比D原子形成的离子少一个电子层.C与B可形成BC型的离子化合物.E的原子序数为29.