摘要:向NaI和Na Br的混合溶液中通入过量的Cl2 .充分反应后将溶液蒸干.灼热残余物.最后剩下的物质是 A.NaCl.I2.Cl2 B. NaCl.I2 C. NaCl.Na Br D. NaCl
网址:http://m.1010jiajiao.com/timu3_id_168695[举报]
完成下列有关反应的化学方程式,并注明有关反应条件:
(1)2-溴丙烷消去反应
(2)苯乙烯的加聚反应
 ;
;
(3)2-甲基-1-丁醇发生消去反应
(4)甲苯与浓硫酸和浓硝酸的混酸反应
 ;
;
(5)向苯酚钠中通入少量CO2
 .
.
查看习题详情和答案>>
(1)2-溴丙烷消去反应
CH3CHBrCH3+NaOH
CH3CH=CH2↑NaBr+H2O
| 乙醇 |
| △ |
CH3CHBrCH3+NaOH
CH3CH=CH2↑NaBr+H2O
;| 乙醇 |
| △ |
(2)苯乙烯的加聚反应


(3)2-甲基-1-丁醇发生消去反应
CH3CH2CH(CH3)CH2OH
CH3CH2C(CH3)=CH2↑+H2O
| 浓硫酸 |
| △ |
CH3CH2CH(CH3)CH2OH
CH3CH2C(CH3)=CH2↑+H2O
;| 浓硫酸 |
| △ |
(4)甲苯与浓硫酸和浓硝酸的混酸反应


(5)向苯酚钠中通入少量CO2


 (1)下列关于实验操作的叙述中正确的为
(1)下列关于实验操作的叙述中正确的为②⑤⑥⑦
②⑤⑥⑦
.(填序号)①从试剂瓶中取出的任何药品,若有剩余,不能再放回原试剂瓶
②可燃性气体点燃之前必须先验纯
③用胶头滴管向试管中滴加液体时,一定要将滴管伸入试管中
④在中和滴定的实验过程中,目光应注视滴定管中液面的变化
⑤蒸馏时,应使温度计水银球与蒸馏烧瓶支管口在同一水平线上
⑥分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
⑦配制浓硫酸和浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中,并及时搅拌和冷却
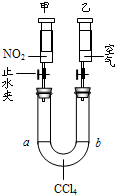
(2)在常温、常压下,注射器甲中装有NO2气体,注射器乙中装有同体积的空气(如图所示,夹持仪器均已略去).
①常温下,打开两个止水夹后,同时向外拉动两注射器的活塞,且拉动的距离相同,将会看到U型管中液面a
下降
下降
(升高、下降、不变);②如将注射器甲中的气体换成NH3,U型管中的CCl4换成水,仍在常温下,打开两个止水夹后,同时向里推动两注射器的活塞,且推动的距离相同,将会看到U型管中液面a
上升
上升
(升高、下降、不变).(3)下列仪器和装置,经过简单连接,可制备中学化学常见的多种不同的气体(暂不考虑尾气的吸收).
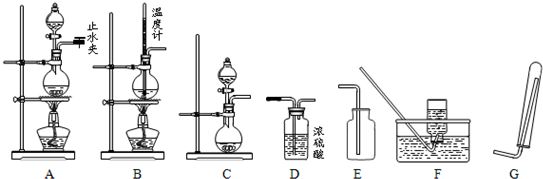
请回答下列问题:
(1)检验A装置气密性的操作为
关闭A装置的止水夹和分液漏斗的旋塞,向分液漏斗中加水.然后打开分液漏斗的旋塞,当少许水进入烧瓶后滴水停止,说明装置A不漏气
关闭A装置的止水夹和分液漏斗的旋塞,向分液漏斗中加水.然后打开分液漏斗的旋塞,当少许水进入烧瓶后滴水停止,说明装置A不漏气
.(2)若用橡胶管连接了装置“B→F”,可制备的气体为
CH2=CH2
CH2=CH2
.(3)若用橡胶管连接了装置“C→D→G”,可制备的气体为
H2
H2
.(4)若用橡胶管连接了装置“C→D→E”,则实验室制备该气体时发生反应的离子方程式为
CaCO3+2H+=Ca2++CO2↑+H2O
CaCO3+2H+=Ca2++CO2↑+H2O
.向NaI和NaBr的混合溶液中通入过量的Cl2,充分反应后,将溶液蒸干、灼烧残留物,最后剩余的物质是( )
| A.NaCl、I2、Cl2 | B.NaCl、I2 | C.NaCl、NaBr | D.NaCl |
(14分)(1)向盛有25 mL 0.2 mol /L的Na2CO3溶液的试管中缓缓滴入0.1 mol /L盐酸75 mL,且边加边振荡,则在标况下产生CO2气体的体积为 mL
(2)FeCl3溶液中混有FeCl2,写出除杂试剂的化学式为 ;反应的离子方程式为
(3)FeCl2溶液中混有FeCl3,写出能检验杂质离子的离子方程式
(4)2.1克平均式量为7.2的CO和H2组成的混和气体在足量的氧气中充分燃烧后,立即通入足量的Na2O2粉未中,待反应完全后,粉末质量可增加 g
(5)1mol Na2O2与足量的CO2完全反应,转移电子的物质的量为
(6)Fe(OH)2转化为Fe(OH)3的现象为 化学方程式为
查看习题详情和答案>>