摘要:23 3Cu+8H++2 NO3-=3Cu2++2NO↑+4H2O (2)25 1.806×1024(3×6.02×1023,3NA) 9624. 2Al+3I22AlI3 催化剂 25Cu , CuCl2 , Cu(OH)2 ,CuO 2) a) Cu+Cl2 △ CuCl2 (若没注明条件扣1分.没配平不给分) b) Fe+ CuCl2=Cu+FeCl2 26. 2F2+2H2O=4HF+O2 ( 2) Ca(ClO)2+CO2+H2O=CaCO3+2HclO 2HClO====2HCl+O2↑. ( 3) 2Na2O2+2CO2=2Na2CO3+O2 氧气
网址:http://m.1010jiajiao.com/timu3_id_166689[举报]
(1)有一种叫做钾长石(K2Al2Si6O16),其化学式为写成氧化物的形式为
(2)反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 的离子方程式为:
每生成11.2L标准状况下的气体,被还原的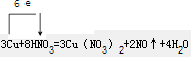
 ;
;
(3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应①A+H2O→B+C ②C+F→D ③D+NaOH
F+E+H2O写出A、B、C的化学式A
查看习题详情和答案>>
K2O?Al2O3?6SiO2
K2O?Al2O3?6SiO2
;(2)反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 的离子方程式为:
3Cu+8H++2NO3?=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3?=3Cu2++2NO↑+4H2O
;每生成11.2L标准状况下的气体,被还原的
硝酸
硝酸
(填名称)的质量为31.5g
31.5g
.得电子与失电子个数比是1:1
1:1
,被氧化与被还原的原子的个数比为3:2
3:2
,试用“单线桥”标出该反应电子转移方向和数目:

(3)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应①A+H2O→B+C ②C+F→D ③D+NaOH
| △ |
NO2
NO2
BNO
NO
CHNO3
HNO3
;写出反应③的离子方程式NH4++OH-
NH3+H2O
| ||
NH4++OH-
NH3+H2O
.
| ||
 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状.
Ⅲ.按如图所示装置连接仪器、检查气密性、装入化学试剂.
(1)过程I发生反应的离子方程式是
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
Cu2(OH)2CO3+4H+═2Cu2++CO2↑+3H2O
.(2)写出过程Ⅲ中检查气密性的方法
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
打开b和a,关闭分液漏斗的活塞,将左边导管插入盛水的烧杯中,轻轻拉动注射器活塞,若导管中液面上升则说明气密性好
.(3)过程Ⅲ的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是
产生红棕色气体
产生红棕色气体
,一段时间后使反应停止的操作是轻轻将注射器活塞向右拉使铜丝和溶液分开
轻轻将注射器活塞向右拉使铜丝和溶液分开
,关闭a,取下注射器.②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生.稀硝酸充满玻璃管的实验目是
将玻璃管中的NO2和空气排出
将玻璃管中的NO2和空气排出
,该反应的离子方程式是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如表所示(忽略温度对气体体积的影响):
| 实验编号 | 水温/℃ | 液面上升高度 | ||
| 1 | 25 | 超过试管的
| ||
| 2 | 50 | 不足试管的
| ||
| 3 | 0 | 液面上升超过实验1 |
低
低
(填“高”或“低”),进入试管中的溶液越多.②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2=HNO3+2NO↑+H2O;
b.HNO2不稳定.
则产生上述现象的原因是
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
温度低,HNO2分解量减少,分解产生的NO气体量减少,所以进入试管的溶液多
.A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大. A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素.F元素原子M层上电子数比L层少2个电子. 试完成下列填空
(1)E元素位于周期表的第
(2)F简单阴离子的结构示意图
 .
.
(3)A、C、D 三种元素共同形成的化合物的电子式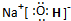
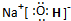 ,其微粒间存在的化学键有
,其微粒间存在的化学键有
(4)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为
(5)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量.离子方程式为
查看习题详情和答案>>
(1)E元素位于周期表的第
三
三
周期ⅢA
ⅢA
族.(2)F简单阴离子的结构示意图


(3)A、C、D 三种元素共同形成的化合物的电子式
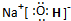
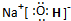
离子键、共价键
离子键、共价键
.(4)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(5)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量.离子方程式为
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
.某化学兴趣小组在实验室探究氨的有关性质,设计了如图所示实验,A处是气体发生装置,A中所用的实验药品从下列物质中选取.
①碳酸钠 ②碳酸氢钠 ③碳酸氢铵④氯化铵 ⑤熟石灰 ⑥氢氧化钠

按图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯,部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)若A中制取气体时只用了一种药品,则该药品是
(2)B装置的作用为
(3)D中铜片发生反应的离子方程式为
A.Na2CO3 B.AgNO3 C. H2SO4 D.FeSO4
(4)图E中持续通入氧气的作用为
(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进,谈谈你的意见:
查看习题详情和答案>>
①碳酸钠 ②碳酸氢钠 ③碳酸氢铵④氯化铵 ⑤熟石灰 ⑥氢氧化钠

按图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯,部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)若A中制取气体时只用了一种药品,则该药品是
③
③
(填物质序号)(2)B装置的作用为
吸收二氧化碳和水蒸气并产生氧气
吸收二氧化碳和水蒸气并产生氧气
(3)D中铜片发生反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的BC
BC
(填下列各项序号)A.Na2CO3 B.AgNO3 C. H2SO4 D.FeSO4
(4)图E中持续通入氧气的作用为
使有害气体吸收更完全
使有害气体吸收更完全
.(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进,谈谈你的意见:
D装置的液体易倒流如玻璃管C中,使玻璃管破裂,在C与D装置之间连接一个防止倒吸的装置
D装置的液体易倒流如玻璃管C中,使玻璃管破裂,在C与D装置之间连接一个防止倒吸的装置
.(2013?淮南一模)A,B,C,D,E为前四周期中原子序数依次增大的元素,相关的信息如下:
请用对应的元素符号回答下列问题:
(1)A与氢可形成一种分子式为A2H4的化合物,该分子中存在σ键和π键数目比为
(2)H-A,H-B两种共价键中,键能较大的是
(3)E位于周期表中的位置是
(4)根据下列能量变化示意图1,请写出BO和AO2反应的热化学方程式
(5)C的最高价氧化物对应的水化物为M,M中含有的化学键类型为

查看习题详情和答案>>
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是客气中含量最丰富的元素 |
| C | 短周期元素中,C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |
(1)A与氢可形成一种分子式为A2H4的化合物,该分子中存在σ键和π键数目比为
5:1
5:1
;(2)H-A,H-B两种共价键中,键能较大的是
H-C
H-C
;H-A,H-D两种共价键中,键的极性较强的是H-Cl
H-Cl
;(3)E位于周期表中的位置是
第四周期第IB族
第四周期第IB族
,单质E与B的最高价氧化物的水化物的稀溶液反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
;(4)根据下列能量变化示意图1,请写出BO和AO2反应的热化学方程式
NO(g)+CO2(g)=NO2(g)+CO(g)△H=+234kJ/mol
NO(g)+CO2(g)=NO2(g)+CO(g)△H=+234kJ/mol
;(5)C的最高价氧化物对应的水化物为M,M中含有的化学键类型为
离子键、极性键
离子键、极性键
,将一定量的D2通入一定浓度M的水溶液中,两者恰好完全反应时,生成物中有三种含D元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如图2所示,请写出t2时刻总反应的化学方程式