摘要:20.图表法.图象法是常用的科学研究方法. (1)短周期某主族元素M的逐级电离能如图(A)所示.则M元素位于周期表的第 ▲ 族. (2)图B是研究部分元素的氢化物的沸点变化规律的图像.折线c可以表达出第 ▲ 族元素氢化物的沸点的变化规律.不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b.你认为正确的是: ▲ .理由是: ▲ . (3)下表列出了一些共价键的键长 C-F C-Cl C-Br C-I C-C C-Si 键长/pm 98 161 182 204 154 170 则CF4.CCl4.CBr4.CI4四种物质中热稳定性最强的是 ▲ .沸点最高的是 ▲ .
网址:http://m.1010jiajiao.com/timu3_id_166585[举报]
图表法、图象法是常用的科学研究方法.
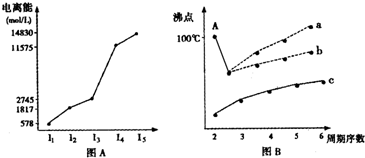
(1)I.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第
II.图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
(2)部分有机物的熔沸点见下表:
由这些数据你能得出的结论是(至少写2条):
查看习题详情和答案>>

(1)I.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第
IIIA
IIIA
族.II.图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
IVA
IVA
族元素氢化物的沸点的变化规律.不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是a还是b?并说出理由:b;A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点
b;A点所示的氢化物是水,由于在水分子间存在氢键,所以其沸点高于氧族元素中的其它氢化物的沸点
.(2)部分有机物的熔沸点见下表:
| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |  |
 |
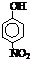 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
同系物相对分子质量越大、分子间作用力越强,故沸点越高
同系物相对分子质量越大、分子间作用力越强,故沸点越高
,当有机能形成分子内氢键时,分子间作用力减弱,熔点变低(当分子间能形成氢键时,分子间作用力增强,熔点升高)
当有机能形成分子内氢键时,分子间作用力减弱,熔点变低(当分子间能形成氢键时,分子间作用力增强,熔点升高)
. 图表法、图象法是常用的科学研究方法.
图表法、图象法是常用的科学研究方法.(Ⅰ)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量.从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推.
现有5种元素L、M、N、O、P,其I1~I3分别如下表,根据表中数据判断其中的金属元素有
M、N、O
M、N、O
,稀有气体元素是P
P
,最活泼的金属是M
M
,显二价的金属是O
O
.| 元 素 | I1/eV | I2/eV | I3/eV |
| L | 13.0 | 23.9 | 40.0 |
| M | 4.3 | 31.9 | 47.8 |
| N | 5.7 | 47.4 | 71.8 |
| O | 7.7 | 15.1 | 80.3 |
| P | 21.6 | 41.1 | 65.2 |
(1)该反应的化学方程式为
2P+3Q?2M
2P+3Q?2M
(2)若M、P、Q均为气体,反应达平衡时:
①体系的压强是开始时的
| 13 |
| 16 |
| 13 |
| 16 |
0.02mol/L?min
0.02mol/L?min
②若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为
放热
放热
反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均分子量比原平衡时减小
减小
(填增大、减小或相等).(3)此反应达平衡后,若只加大体系压强,M的物质的量增加,若M是气体,则Q的聚集状态是
气态
气态
.
图表法、图象法是常用的科学研究方法.阅读下列图表回答问题:
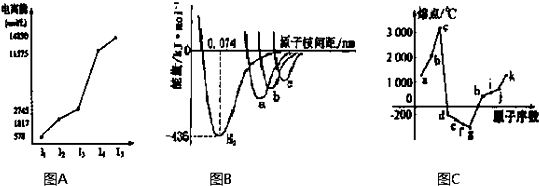
(1)图A是第三周期某主族元素M的电离能变化情况的图象.则M元素位于周期表的 族,根据同周期元素第一电离能的变化规律,推断在M元素所在周期的所有元素中,M元素的第一电离能的大小(最小)范围为 <M< (填元素符号).
(2)图B是表示H2、Cl2、Br2、I2四种分子形成过程中能量随核间距的变化情况的图象,其中表示I2的曲线的是 (填“a”、“b”、“c”),理由是 .
(3)图C是1~18号元素中部分连号元素单质的熔点变化情况图,其中c点代表的单质是 ,其熔点高的主要原因是 .
查看习题详情和答案>>

(1)图A是第三周期某主族元素M的电离能变化情况的图象.则M元素位于周期表的
(2)图B是表示H2、Cl2、Br2、I2四种分子形成过程中能量随核间距的变化情况的图象,其中表示I2的曲线的是
(3)图C是1~18号元素中部分连号元素单质的熔点变化情况图,其中c点代表的单质是
(11分)图表法、图象法是常用的科学研究方法。阅读下列图表回答问题:
(1)第三周期某主族元素M的电离能情况如图(A)所示。则M元素位于周期表的_____族,根据同周期元素第一电离能的变化规律,推断在M元素所在周期的所有元素中,M元素的第一电离能的大小(最小)范围为______<M<________(填元素符号)。
(2)图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第_______族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是:______(填“a”或“b”),请说明A点代表的的氢化物的沸点较高的原因_____________________________________________。
(3) 图C是表示表示第三周期8种元素单质的熔点(℃)折线图,已知序号“1”对应的点代表Ar,其中序号“8”代表 _______(填元素符号);其中电负性最大的是_________(填图C中的序号)。
查看习题详情和答案>>
(12分)图表法、图象法是常用的科学研究方法。
下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 | A | B[ | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)已知H为Na元素,则以上10种元素中第一电离能最小的是: (填编号)。比元素B原子序数大10的元素其基态原子的核外电子排布是
 。
。(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是 (写分子式,写出一种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其一分子中共形
成
 个σ键, 个π键。
个σ键, 个π键。(4)短周期某主族元素K的电离能情况如图(A)所示。
则K元素位于周期表的第 族。

图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线—折线a和折线b,你认为正确的是 ,理由是 查看习题详情和答案>>