摘要:24.在反应C12+2KI==2KCl+I2中.失去电子的是 A.Cl2中的Cl B.KI中的I C.KCl中的Cl D.I2中的I
网址:http://m.1010jiajiao.com/timu3_id_165950[举报]
下列有关说法正确的是(设NA为阿伏伽德罗常数的值)( )
查看习题详情和答案>>
| A.向氯水中加入NaOH溶液至中性,所得溶液中c(Na+)=c(Cl-)+c(ClO-) |
| B.Na2O2在空气中长期放置,最终变为NaHCO3粉末 |
| C.某溶液中加入铝粉能产生氢气,该溶液中可能大量存在:H+、SO42-、NO3-、Na+ |
| D.在反应O3+2KI+H2O═2KOH+I2+O2中,每生成32gO2,转移电子数目为NA |
下列有关说法正确的是(设NA为阿伏伽德罗常数的值)( )
A.向氯水中加入NaOH溶液至中性,所得溶液中c(Na+)=c(Cl-)+c(ClO-)
B.Na2O2在空气中长期放置,最终变为NaHCO3粉末
C.某溶液中加入铝粉能产生氢气,该溶液中可能大量存在:H+、SO42-、NO3-、Na+
D.在反应O3+2KI+H2O═2KOH+I2+O2中,每生成32gO2,转移电子数目为NA
查看习题详情和答案>>
A.向氯水中加入NaOH溶液至中性,所得溶液中c(Na+)=c(Cl-)+c(ClO-)
B.Na2O2在空气中长期放置,最终变为NaHCO3粉末
C.某溶液中加入铝粉能产生氢气,该溶液中可能大量存在:H+、SO42-、NO3-、Na+
D.在反应O3+2KI+H2O═2KOH+I2+O2中,每生成32gO2,转移电子数目为NA
查看习题详情和答案>>
下列有关说法正确的是(设NA为阿伏伽德罗常数的值)
- A.向氯水中加入NaOH溶液至中性,所得溶液中c(Na+)=c(Cl-)+c(ClO-)
- B.Na2O2在空气中长期放置,最终变为NaHCO3粉末
- C.某溶液中加入铝粉能产生氢气,该溶液中可能大量存在:H+、SO42-、NO3-、Na+
- D.在反应O3+2KI+H2O═2KOH+I2+O2中,每生成32gO2,转移电子数目为NA
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如下图:
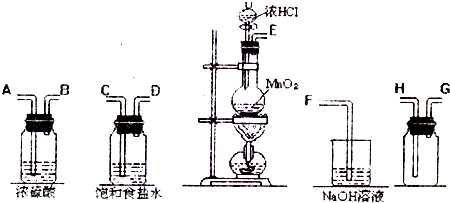
(1)连接上述仪器的正确顺序是(填各接口处的字母):E接
(2)在装置中;①饱和食盐水起的作用是
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸.如果有Cl2产生,可观察到的现象是
(4)写出下列化学反应的离子方程式
①气体发生装置中进行的反应:
②尾气吸收装置中进行的反应:
查看习题详情和答案>>

(1)连接上述仪器的正确顺序是(填各接口处的字母):E接
C
C
,D
D
接A
A
,B
B
接H,G接F.(2)在装置中;①饱和食盐水起的作用是
除去挥发出的HCl气体,抑制C12在水中的溶解
除去挥发出的HCl气体,抑制C12在水中的溶解
;②浓硫酸起的作用是吸收水蒸气,干燥Cl2
吸收水蒸气,干燥Cl2
.(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸.如果有Cl2产生,可观察到的现象是
白色试纸变蓝
白色试纸变蓝
,写出反应方程式2KI+Cl2=2KCl+I2
2KI+Cl2=2KCl+I2
.(4)写出下列化学反应的离子方程式
①气体发生装置中进行的反应:
MnO2+4H++2C1-
Mn2++C12↑+2H2O
| ||
MnO2+4H++2C1-
Mn2++C12↑+2H2O
;
| ||
②尾气吸收装置中进行的反应:
C12+2OH-=ClO-+C1-+H2O
C12+2OH-=ClO-+C1-+H2O
.