摘要:20. (1)铝热反应在工业生产上有重要应用.如焊接钢轨.焊接大截面钢材部件等.请写出铝与三氧化二铁反应的化学方程式 . (2)检验溶液中Fe3+存在的试剂是 .证明Fe3+存在的现象是 .电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔.制造印刷电路板.写出该瓜的离子方程式 . 21.下图表示某些物质之间的转化关系.每个字母代表一种物质.部分产物已略去.A是一种酸式盐.也是一种常用的化学肥料.B是能使湿润的红色石蕊试纸变蓝色的无色气体.D是无色无味气体. 回答下列问题: (1)物质A的名称是 . (2)写出物质B的一种主要用途 . (3)写出实验室制取气体B的化学方程式 . 写出工业上制取气体B的化学方程式 . (4)写出反应的化学方程式: B→E . F→G .
网址:http://m.1010jiajiao.com/timu3_id_164050[举报]
化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。(1) 铝热反应在工业生产中的重要用途之一是 ;用化学方程式表示出其中的原理 (举一例)。铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若将氧化铝与氢氧化钠溶液作用,反应的化学方程式为 。
(2)氯气用于漂白、消毒时,能起漂白、消毒作用的物质是 (写化学式)。缺铁性贫血患者应补充Fe元素,通常以硫酸亚铁的形式给药,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是
。(用化学方程式表示)。
(4)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3 C = 2AlN + 3CO
①在化学方程式上标出该反应中电子转移的方向和数目。
②在该反应中,氧化剂是 ,氧化产物是 。
查看习题详情和答案>>
学习化学应该明确“从生活中来,到生活中去”道理.在生产生活中,我们会遇到各种各样的化学反应.请按要求回答下列问题:
(1)写出下列反应的化学方程式.(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是 .
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉 .
(2)请你写出下列反应的离子方程式.
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多 .
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板 .
(3)工业上生产半导体材料硅的流程如图:
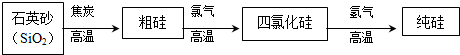
写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目: .
(4)铝热反应在工业生产中的重要用途之一是 ;小苏打在日常生活中的用途之一是 ,将小苏打和纯碱的混合物19.0g加热到恒重,测得固体质量为15.9g,则混合物中小苏打的质量分数为 .
查看习题详情和答案>>
(1)写出下列反应的化学方程式.(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉
(2)请你写出下列反应的离子方程式.
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板
(3)工业上生产半导体材料硅的流程如图:

写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目:
(4)铝热反应在工业生产中的重要用途之一是
请按要求回答下列问题:
(1)铝热反应在工业生产中的重要用途之一是 ;
(2)氯气是一种重要的化工原料,工业上用电解饱和食盐水制氯气,写出该反应的化学方程式 .
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是(用化学方程式表示) .
查看习题详情和答案>>
(1)铝热反应在工业生产中的重要用途之一是
(2)氯气是一种重要的化工原料,工业上用电解饱和食盐水制氯气,写出该反应的化学方程式
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是(用化学方程式表示)