摘要:关于原子结构的叙述正确的是 A.所有的原子核都是由质子和中子组成的 B.原子的最外层电子数不超过8个 C.稀有气体原子的最外层电子数均为8 D.原子的次外层电子数都是8
网址:http://m.1010jiajiao.com/timu3_id_163239[举报]
下列有关叙述正确的是
A.稀有气体的晶体其组成微粒是原子,晶体中不存在分子间作用力
B.金刚石的熔、沸点高于晶体硅,因为C—C键能大于Si—Si键能
C.CO燃烧的热化学方程式可表示为:CO(g)+![]() O2(g)
O2(g)![]() CO2(g);ΔH=+283 kJ·mol-1
CO2(g);ΔH=+283 kJ·mol-1
D. C-12的原子组成符号为![]() C,二氧化碳分子的结构式为O=C=O
C,二氧化碳分子的结构式为O=C=O
 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:(1)若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
①A中所含有的化学键是
离子键和共价键
离子键和共价键
.②将4.48L(标准状况下)X通入100mL 3mol/L A的水溶液后,溶液中离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L.若取相同质量的固体加热至恒重,剩余固体的质量为
2.65
2.65
.(2)若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构.
①下列有关B物质的叙述正确的是
bc
bc
a、B的分子式为AX b、B为共价化合物
c、B分子呈三角锥形 d、B性质稳定,不与除X外的任何物质发生化学反应
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为
PCl5+4H2O=H3PO4+5HC1
PCl5+4H2O=H3PO4+5HC1
.下列有关叙述正确的是( )
| A、稀有气体的晶体其组成微粒是原子,晶体中不存在分子间作用力 | ||
| B、金刚石的熔沸点高于晶体硅,因为C-C键能大于Si-Si键能 | ||
C、CO燃烧的热化学方程式可表示为:CO(g)+
| ||
D、C-12的原子组成符号为
|
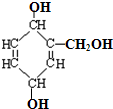 关于结构如图所示的有机物的叙述中正确的是( )
关于结构如图所示的有机物的叙述中正确的是( )