题目内容
 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:(1)若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
①A中所含有的化学键是
离子键和共价键
离子键和共价键
.②将4.48L(标准状况下)X通入100mL 3mol/L A的水溶液后,溶液中离子浓度由大到小的顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
.③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L.若取相同质量的固体加热至恒重,剩余固体的质量为
2.65
2.65
.(2)若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构.
①下列有关B物质的叙述正确的是
bc
bc
a、B的分子式为AX b、B为共价化合物
c、B分子呈三角锥形 d、B性质稳定,不与除X外的任何物质发生化学反应
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为
PCl5+4H2O=H3PO4+5HC1
PCl5+4H2O=H3PO4+5HC1
.分析:(1)若A、B、C的焰色反应均呈黄色,水溶液均为碱性,则A为氢氧化钠,X为二氧化碳,根据转化关系知B为碳酸钠,C为碳酸氢钠;
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构,由转化关系可知,A为磷,B为三氯化磷,C为五氯化磷,x为氯气.
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构,由转化关系可知,A为磷,B为三氯化磷,C为五氯化磷,x为氯气.
解答:解:(1)若A、B、C的焰色反应均呈黄色,水溶液均为碱性,则A为氢氧化钠,X为二氧化碳,根据转化关系知B为碳酸钠,C为碳酸氢钠,
①A为氢氧化钠,属于离子化合物,钠离子与氢氧根离子之间形成离子键,氢氧根离子中氧原子与氢原子之间形成1对共用电子对,为共价键,属于A中所含有的化学键是 离子键、共价键.
故答案为:离子键、共价键.
②n (CO2)=0.2mol,n(NaOH)=0.3mol,
则反应的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,
则有:2>
=
>1,
所以:所得产物为Na2CO3和NaHCO3,
设所得产物中含Na2CO3为xmol,NaHCO3为ymol,
则得方程组:
解得:x=0.1,y=0.1,在含等物质的量的碳酸钠、碳酸氢钠的溶液中,c(Na+)最大,碳酸根离子水解大于碳酸氢根离子的水解,则c(HCO3-)>c(CO32-),
水解使溶液显碱性,则c(OH-)>c(H+),显性离子大于隐性离子,所以c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
即离子浓度大小为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L,即钠离子浓度为0.5mol/L.取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为
×0.1L×0.5mol/L×106g/mol=2.65g.
故答案为:2.65;
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构,由转化关系可知,A为磷,B为三氯化磷,C为五氯化磷,x为氯气.
①B是三氯化磷,
a、B的分子式为PCl3,故A错误;
b、三氯化磷为共价化合物,故正确;
c、三氯化磷分子中磷原子含有3个共价单键和一个孤电子对,其空间构型是三角锥型,故错误;
d、三氯化磷能和环氧乙烷反应,故错误;
②C为五氯化磷,与水剧烈反应,生成磷酸和盐酸,反应的化学方程式为PCl5+4H2O=H3PO4+5HC1.
故答案为:PCl5+4H2O=H3PO4+5HC1.
①A为氢氧化钠,属于离子化合物,钠离子与氢氧根离子之间形成离子键,氢氧根离子中氧原子与氢原子之间形成1对共用电子对,为共价键,属于A中所含有的化学键是 离子键、共价键.
故答案为:离子键、共价键.
②n (CO2)=0.2mol,n(NaOH)=0.3mol,
则反应的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,
则有:2>
| n(NaOH) |
| n(CO2) |
| 3 |
| 2 |
所以:所得产物为Na2CO3和NaHCO3,
设所得产物中含Na2CO3为xmol,NaHCO3为ymol,
则得方程组:
|
解得:x=0.1,y=0.1,在含等物质的量的碳酸钠、碳酸氢钠的溶液中,c(Na+)最大,碳酸根离子水解大于碳酸氢根离子的水解,则c(HCO3-)>c(CO32-),
水解使溶液显碱性,则c(OH-)>c(H+),显性离子大于隐性离子,所以c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
即离子浓度大小为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L,即钠离子浓度为0.5mol/L.取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为
| 1 |
| 2 |
故答案为:2.65;
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构,由转化关系可知,A为磷,B为三氯化磷,C为五氯化磷,x为氯气.
①B是三氯化磷,
a、B的分子式为PCl3,故A错误;
b、三氯化磷为共价化合物,故正确;
c、三氯化磷分子中磷原子含有3个共价单键和一个孤电子对,其空间构型是三角锥型,故错误;
d、三氯化磷能和环氧乙烷反应,故错误;
②C为五氯化磷,与水剧烈反应,生成磷酸和盐酸,反应的化学方程式为PCl5+4H2O=H3PO4+5HC1.
故答案为:PCl5+4H2O=H3PO4+5HC1.
点评:本题考查元素化合物推断,难度中等,关键掌握常见元素化合物的性质,根据转化关系选择合适的物质进行解答.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
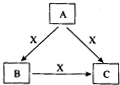 A、B、C、X是中学化学常见物质,转化关系如图所示.请针对以下不同情况回答问题:
A、B、C、X是中学化学常见物质,转化关系如图所示.请针对以下不同情况回答问题: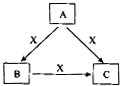 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下三种不同情况回答:
 A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去).请回答下列问题:
A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去).请回答下列问题: A、B、C、X是中学化学中常见的物质,它们之间的转化关系如下图所示(部分产物已略去).请回答下列问题:
A、B、C、X是中学化学中常见的物质,它们之间的转化关系如下图所示(部分产物已略去).请回答下列问题: