摘要:含d g Ag+的AgNO3溶液与足量NaCl溶液反应.得e g沉淀.已知银的相对原子质量为108.则氯原子的摩尔质量为 .
网址:http://m.1010jiajiao.com/timu3_id_162797[举报]
四川有丰富的天然气资源.某化工厂以天然气为原料合成氨的工艺流程示意图如下:
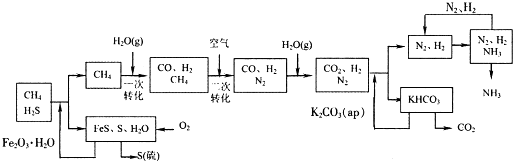
依据上述流程,完成下列填空:
(1)整个流程有三个循环:一是K2CO3(aq)循环,二是N2和H2循环,第三个循环中被循环的物质是
(2)脱硫过程中,若有nmol Fe2O3?H2O转化,则生成S的物质的量为 mol(用含n的代数式表示).
(3)图中CH4的第二次转化过程中发生反应的化学方程式为 .
(4)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气.请运用化学反应速率和化学平衡的观点说明采取这些措施的理由:
(5)改用过量NaOH溶液吸收天然气中的硫化氢,以石墨作电极电解吸收后所得溶液可回收硫,其电解总反应方程式(忽略氧气的氧化还原)为
(6)若工业生产中以a g氨气和足量的空气为原料(不考虑空气中N2的反应)最大限度的制取NH4NO3,经过一系列转化后,再向反应后的混合物中加入bg水,得到密度为d g/mL的NH4NO3溶液,理论上该溶液中溶质的物质的量浓度可能的最大值为 mol/L.
查看习题详情和答案>>

依据上述流程,完成下列填空:
(1)整个流程有三个循环:一是K2CO3(aq)循环,二是N2和H2循环,第三个循环中被循环的物质是
(2)脱硫过程中,若有nmol Fe2O3?H2O转化,则生成S的物质的量为
(3)图中CH4的第二次转化过程中发生反应的化学方程式为
(4)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气.请运用化学反应速率和化学平衡的观点说明采取这些措施的理由:
(5)改用过量NaOH溶液吸收天然气中的硫化氢,以石墨作电极电解吸收后所得溶液可回收硫,其电解总反应方程式(忽略氧气的氧化还原)为
(6)若工业生产中以a g氨气和足量的空气为原料(不考虑空气中N2的反应)最大限度的制取NH4NO3,经过一系列转化后,再向反应后的混合物中加入bg水,得到密度为d g/mL的NH4NO3溶液,理论上该溶液中溶质的物质的量浓度可能的最大值为
 金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.
金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.(1)钢铁的表面发蓝、发黑处理是常用的防腐方法.下列反应是主要反应之一.
请配平方程式:
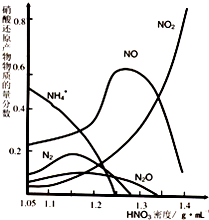
(2)钢铁的“钝化”处理也能达到防腐目的,经冷、浓HNO3处理后,其表面有一层致密氧化物保护膜,但是加热或在稀HNO3中就不能“钝化”.不同浓度的HNO3与铁反应的还原产物很复杂,其分布曲线如图.
①图示可知,密度为1.05g?mL-1的硝酸与铁反应时,其最多的还原产物是
②m g铁与含n g HNO3的硝酸溶液恰好完全反应,若硝酸的还原产物只有NO,则m的取值可能是
A.
| 1 |
| 5 |
| 2 |
| 9 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 2 |
③工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是:
(3)金属M的腐蚀是因为发生反应:M-ne-→Mn+,除了上述表面处理的方法外,下列方法也能起到防腐作用的是
A.在铁中掺入铭、镇等金属,改变其内部结构,制成不锈钢
B.在铁制品表面镀锌
C.提高铁中含碳量,制成生铁
D.将水库铁闸门与直流电源的负极相连.