网址:http://m.1010jiajiao.com/timu3_id_162618[举报]
(1)写出原子序数最小的第Ⅷ族元素原子的原子结构示意图为:
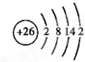

(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是
(4)第三主族的元素由于最外能层的p能级中有空轨道,故称为缺电子元素.硼酸的结构式可表示为
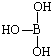 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:(5)写出二氧化硫和水合氢离子中硫原子,氧原子分别采用
(6)已知N-N,N=N,N≡N键能之比为1.00:2.17:4.90,而C-C,C=C,C≡C键能之比为1.00:1.77:2.34.用数据分析氮分子不容易发生加成反应而乙烯和乙炔容易发生加成反应的原因
(7)用氢键表示法表示邻羟基苯甲醛分子内氢键


卤族元素的单质和化合物很多,请利用所学物质结构与性质的相关知识回答下列问题:
(1)卤族元素位于周期表的 ????????? 区;氟原子的电子排布图为?????? 溴原子的价电子排布式为????? .
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是??????????
(3)已知高碘酸有两种形式,化学式分别为H5IO6 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6??????????? HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为???????????? 。
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大。这是由于溶液中发生下列反应 I-+ I2 =I3-与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 ??? 式发生。
A.CsICl2=CsCl+ICl?????? B.CsICl2 =CsI +Cl2
(5)ClO2-的空间构型为?????? 型,中心氯原子的杂化轨道类型为???????? ,写出一个ClO2-的等电子体 ???????????? 。
(6)如图为碘晶体晶胞结构。有关说法中正确的是???? 。

A.碘分子的排列有2种不同的取向
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3 .NA为阿伏加德罗常数,相邻的两个Ca2+核间距为a cm,则CaF2的摩尔质量可以表示为?????? 。
查看习题详情和答案>>
(1)卤族元素位于周期表的 区;氟原子的电子排布图为 溴原子的价电子排布式为 .
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是
(3)已知高碘酸有两种形式,化学式分别为H5IO6
 和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6 HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为 。
和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱: H5IO6 HIO4.(填“>”、“<”或“=”)。H5IO6中α键与π键的个数比为 。(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大。这是由于溶液中发生下列反应 I-+ I2 =I3-与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生。
A.CsICl2=CsCl+ICl B.CsICl2 ="CsI" +Cl2
(5)ClO2-的空间构型为 型,中心氯原子的杂化轨道类型为 ,写出一个ClO2-的等电子体 。
(6)如图为碘晶体晶胞结构。有关说法中正确的是 。

A.碘分子的排列有2种不同的取向
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
(7)已知CaF2晶体(见图)的密度为ρg/cm3.NA为阿伏加德罗常数,相邻的两个Ca2+核间距为a cm,则CaF2的摩尔质量可以表示为 。
某校合作探究小组利用业余时间上网搜索烯类化合物与溴加成反应的有关信息,获得的有关结构与数据列表如下(以乙烯为标准)

(1)据表中数据,总结烯类化合物加溴时,反应速率与碳碳双键上取代基的种类、个数间的关系:________.
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是________.
A.(CH3)2C=C(CH3)2
B.CH3CH=CHCH3
C.CH2=CH2
D.CH2=CHCl
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸(![]() )、乙酸分子中羟基上氢原子的活泼性.
)、乙酸分子中羟基上氢原子的活泼性.
(1)甲同学将一些化学实验收集整理如下:
A.金属钠分别与水和乙醇反应
B.苯酚、二氧化碳、乙酸分别与氢氧化钠溶液反应
C.向二氧化碳水溶液、乙酸溶液中分别滴加紫色石蕊试液
D.将鸡蛋壳破碎后加入到醋酸溶液中
E.向苯酚溶液中滴加FeCl3溶液
F.向苯酚钠溶液中分别通入二氧化碳和滴加盐酸
其中能说明水比乙醇强的是________(填字母,下同),乙酸比碳酸强的是________.
(2)乙同学与其他同学合作,设计了一个简单的一次性完成的实验装置来验证乙酸、碳酸和苯酚溶液的酸性强弱,以说明其羟基上氢原子的活泼性顺序.根据下列实验装置图回答有关问题.

①A对应的仪器名称是________;
②各仪器的连接顺序是(填数字,仪器可重复使用)________;
③饱和NaHCO3溶液作用是________;
④实验过程中观察到的现象有________.
(Ⅰ)某校合作探究小组利用业余时间上网搜索烯类化合物与溴加成反应的有关信息,获得的有关结构与数据列表如下(以乙烯为标准)
| 烯 类 化 合 物 | 相 对 速 率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
(1)据表中数据,总结烯类化合物加溴时,反应速率与碳碳双键上取代基的种类、个数间的关系:___________________________ ______ 。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是_________。
A.(CH3)2C= C (CH3)2 B.CH3CH=CHCH3 C.CH2=CH2 D.CH2=CHCl
![]() (Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。 O
(1)甲同学将一些化学实验收集整理如下:
A.金属钠分别与水和乙醇反应 B.苯酚、二氧化碳、乙酸分别与氢氧化钠溶液反应
C.向二氧化碳水溶液、乙酸溶液中分别滴加紫色石蕊试液
D.将鸡蛋壳破碎后加入到醋酸溶液中 E.向苯酚溶液中滴加FeCl3溶液
F.向苯酚钠溶液中分别通入二氧化碳和滴加盐酸
其中能说明水比乙醇强的是 (填字母,下同),乙酸比碳酸强的是 。
(2)乙同学与其他同学合作,设计了一个简单的一次性完成的实验装置来验证乙酸、碳酸和苯酚溶液的酸性强弱,以说明其羟基上氢原子的活泼性顺序。根据下列实验装置图回答有关问题。
① A对应的仪器名称是 ;
② 各仪器的连接顺序是(填数字,仪器可重复使用) ;
③ 饱和NaHCO3溶液作用是 ;
④ 实验过程中观察到的现象有 。
查看习题详情和答案>>