摘要:23.甲同学意见不正确.因为空气过多时.多余的空气会带走热量.
网址:http://m.1010jiajiao.com/timu3_id_161943[举报]
学生设计了三个实验方案,用以检验淀粉的水解情况.
方案甲:淀粉液
水解液
中和液
溶液变蓝
结论:淀粉完全没有水解
方案乙:淀粉液
水解液
无银镜现象
结论:淀粉完全没有水解
方案丙:淀粉液
水解液
中和液
有银镜出现
结论:淀粉已经水解
(1)根据上述操作、现象,首先回答结论是否正确,不正确的简要说明理由.
方案甲:
方案乙:
方案丙:
(2)写出淀粉彻底水解的化学方程式
查看习题详情和答案>>
方案甲:淀粉液
| H2SO4 |
| △ |
| NaOH |
| 碘水 |
结论:淀粉完全没有水解
方案乙:淀粉液
| H2SO4 |
| △ |
| 银氨溶液 |
| 微热 |
结论:淀粉完全没有水解
方案丙:淀粉液
| H2SO4 |
| △ |
| NaOH |
| 银氨溶液 |
| 微热 |
结论:淀粉已经水解
(1)根据上述操作、现象,首先回答结论是否正确,不正确的简要说明理由.
方案甲:
结论不正确,因为淀粉可能部分水解,未水解的残留淀粉会与碘反应变蓝
结论不正确,因为淀粉可能部分水解,未水解的残留淀粉会与碘反应变蓝
;方案乙:
结论不正确,因为实验设计有错误,在酸性条件下即使水解液中有葡萄糖,也不能与银氨溶液发生银镜反应
结论不正确,因为实验设计有错误,在酸性条件下即使水解液中有葡萄糖,也不能与银氨溶液发生银镜反应
;方案丙:
结论正确
结论正确
.(2)写出淀粉彻底水解的化学方程式
(C6H10O5)n+nH2O
nC6H12O6
| 稀硫酸 |
(C6H10O5)n+nH2O
nC6H12O6
写出葡萄糖与银氨溶液反应的化学方程式| 稀硫酸 |
CH2OH(CHOH)4CHO+2Ag(NH3)2OH
CH2OH(CHOH)4COONH4+H2O+2Ag+3NH3↑
| 水溶 |
| △ |
CH2OH(CHOH)4CHO+2Ag(NH3)2OH
CH2OH(CHOH)4COONH4+H2O+2Ag+3NH3↑
.该反应的类型为| 水溶 |
| △ |
氧化还原反应
氧化还原反应
.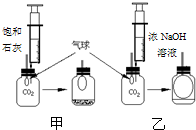 发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液.
发现问题:研究性学习小组中的小张同学在学习中发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液. 实验探究:在体积相同盛满CO2 的两集气瓶中,分别加入等体积的饱和石灰水和浓NaOH 溶液.实验装置和现象如图所示.请你一起参与.
现象结论:甲装置中产生的实验现象(用化学方程式表示)
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
,解释通常用石灰水而不用NaOH 溶液检验CO2的原因CO2与石灰水作用有明显实验现象,NaOH无明显现象
CO2与石灰水作用有明显实验现象,NaOH无明显现象
;乙装置中的实验现象是气球体积增大,溶液不变浑浊
气球体积增大,溶液不变浑浊
,吸收CO2较多的装置是乙
乙
.计算验证:另一位同学小李通过计算发现,等质量的Ca(OH)2和NaOH吸收CO2的质量,Ca(OH)2大于NaOH.因此,他认为通常吸收CO2 应该用饱和石灰水.
思考评价:请你对小李同学的结论进行评价:
不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中
溶质的质量分数很小.
溶质的质量分数很小.
不正确,因为Ca(OH)2的溶解度很小,所形成的饱和石灰水中
溶质的质量分数很小.
.溶质的质量分数很小.
(2009?泰州模拟)高纯超净特种气体主要用于制造半导体器件、化合物半导体、激光器、光导纤维、太阳能电池等.超纯硅化氢制备方法如下:(已知:常温下SiH4难溶于水,与稀硫酸不反应,乙醚沸点34.6℃)
①由下列两种方法制得SiH4
方法一:Mg2Si+4NH4Cl
SiH4+2MgCl2+4NH3
方法二:LiAlH4+SiCl4
SiH4+AlCl3+LiCl
②除去SiH4中混有的杂质气体
请回答下列问题:
(1)对方法一的理解,有同学认为是NH4+水解产生H+,Mg2Si与H+反应生成SiH4,你认为该观点是否正确?并简述理由
(2)将方法二的固体产物溶于水,只有一种物质能促进水的电离,则NaOH、Mg(OH)2、LiOH碱性由强到弱的顺序为
(3)两种方法制得的SiH4中均含有少量杂质,有同学提出用下列方法除去SiH4中的杂质,其中肯定不可行是
a.用稀硫酸洗气 b.高温使杂质分解 c.低温分馏
(4)甲、乙、丙三同学在讨论SiH4制备方法的化学反应类型时发表如下观点,你认为正确的是
a.甲同学认为两个反应均为氧化还原反应
b.乙同学认为两个反应中只有一个属于氧化还原反应
c.丙同学认为要判断是否属于氧化还原反应,还需要知道SiH4中各元素具体的化合价.
查看习题详情和答案>>
①由下列两种方法制得SiH4
方法一:Mg2Si+4NH4Cl
| 液氨 |
方法二:LiAlH4+SiCl4
| C2H5OC2H5 |
②除去SiH4中混有的杂质气体
请回答下列问题:
(1)对方法一的理解,有同学认为是NH4+水解产生H+,Mg2Si与H+反应生成SiH4,你认为该观点是否正确?并简述理由
不正确,因为该反应在液氨中进行,非水体系,不会水解
不正确,因为该反应在液氨中进行,非水体系,不会水解
.(2)将方法二的固体产物溶于水,只有一种物质能促进水的电离,则NaOH、Mg(OH)2、LiOH碱性由强到弱的顺序为
NaOH>LiOH>Mg(OH)2
NaOH>LiOH>Mg(OH)2
.(3)两种方法制得的SiH4中均含有少量杂质,有同学提出用下列方法除去SiH4中的杂质,其中肯定不可行是
b
b
.a.用稀硫酸洗气 b.高温使杂质分解 c.低温分馏
(4)甲、乙、丙三同学在讨论SiH4制备方法的化学反应类型时发表如下观点,你认为正确的是
bc
bc
.a.甲同学认为两个反应均为氧化还原反应
b.乙同学认为两个反应中只有一个属于氧化还原反应
c.丙同学认为要判断是否属于氧化还原反应,还需要知道SiH4中各元素具体的化合价.