摘要:解:根据质量分数的概念: (1) (2)稀释前后盐酸的物质的量相等.即:c1V1 = c2V2 设稀释后的盐酸浓度为c.则: 10×11.8 = 1450×c c = 0.08 mol·L-1
网址:http://m.1010jiajiao.com/timu3_id_160146[举报]
下列说法正确的是( )
| A、19世纪初,化学家维勒提出了有机化学的概念 | B、同位素示踪法是科学家经常使用的研究化学反应历程的手段之一 | C、测定有机化合物中碳、氢元素质量分数的方法最早由维特里希提出的 | D、甲烷与氯气在光照下发生卤代反应,其机理是甲烷在光照条件下形成自由基(CH3.),甲基自由基与氯气分子发生碰撞,从氯气分子中夺一个氯原子,生成一氯甲烷 |
 (2013?中山一模)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
(2013?中山一模)根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:(1)P点表示在t1℃两物质的溶解度关系为b
=
=
c(填“>”、“<”或“=”).(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为
b>a>c
b>a>c
.(3)t2℃时,50g b物质加入到50g水中充分溶解后,所得溶液的质量为
75g
75g
.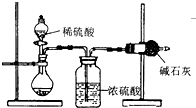 测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:
测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:I.吸收法
如图所示:
(1)根据实验装置图分析,在每次实验过程中所进行的称量操作至少要进行
4
4
次,且第一次称量操作的对象是称量干燥烧瓶的质量
称量干燥烧瓶的质量
.(2)若重复测定了三次,得到Na2CO3的质量分数的数据存在较大的偏差,产生偏差的原因可能是
ACD
ACD
(填序号).A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.用了稀硫酸与样品反应
C.加入稀硫酸的量不足,则可能造成误差
D.反应完成后,装置中仍存有二氧化碳,没有被碱石灰吸收
除上述原因外,从装置看还有一个重要原因是
装置外的空气中的水蒸气和二氧化碳被碱石灰吸收
装置外的空气中的水蒸气和二氧化碳被碱石灰吸收
.II.滴定法
称取样品m g,配制成500mL溶液.从中取出25mL加入足量的BaCl2溶液振荡,滴加2~3滴酚酞,用a mol/L标准盐酸滴定,至终点时消耗盐酸v mL.
(1)该同学加入足量的BaCl2溶液后未将BaCO3过滤就滴定,有人认为在滴定中BaCO3会转化为Ba(HCO3)2,消耗盐酸.你认为要过滤吗?
否
否
(填“是”或“否”),理由是:用酚酞做指示剂到终点时溶液呈微弱的碱性,BaCO3不反应
用酚酞做指示剂到终点时溶液呈微弱的碱性,BaCO3不反应
(若填“是”,不需答).(2)判断滴定终点到达的依据是
当滴入最后一滴盐酸时,溶液立即由浅红色变化为无色,且半分钟内颜色不变化
当滴入最后一滴盐酸时,溶液立即由浅红色变化为无色,且半分钟内颜色不变化
.Ⅲ.沉淀法
称取样品m g,并溶解加过量Ba(NO3)2溶液,过滤、洗涤、烘干,称量得固体n g.
(1)混合物中碳酸钠的质量分数为(用m、n表示)
| 106n |
| 197m |
| 106n |
| 197m |
(2)洗涤沉淀的操作要点是
用玻璃棒向过滤器中的沉淀加水至淹没,静置使水滤出,并重复2-3次
用玻璃棒向过滤器中的沉淀加水至淹没,静置使水滤出,并重复2-3次
.(3)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用Ba(NO3)2溶液而不用Ca(NO3)2溶液的原因是
Ca(OH)2微溶
Ca(OH)2微溶
;测定CO32-的量,若使用Ba(OH)2溶液而不用Ca(OH)2溶液,结果将具有更高的精确度,原因BaCO3相对分子质量大,相对误差小
BaCO3相对分子质量大,相对误差小
.生铁中含碳和硫等元素.化学兴趣小组对某生铁样品成分及其含量进行探究.
Ⅰ.生铁中碳和硫元素的定性检验
(1)将以下装置进行连接以完成实验(夹持仪器已略去,填接口字母代号)
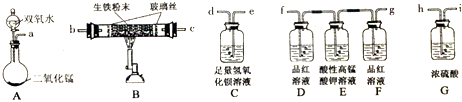
a→ → → → → → →
(2)将样品研磨成粉末的目的是 .
(3)确认样品中含有碳元素的现象是 .
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量.称取样品m1g进行实验,充分反应后,测得C中生成的沉淀为m2g,该样品中碳的质量分数不小于 (用含m1、m2的式子表示)
(5)乙同学认为,待一定量样品充分反应后,向E装置中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案是否合理? (填“是”或“否”);说明理由 .
(6)丙同学提议:为测定样品中硫的含量,可将c装置中试剂改为足量的30%双氧水,并按A→G→B→C装置连接进行实验,充分反应后,请你简述后续的实验方案 .
查看习题详情和答案>>
Ⅰ.生铁中碳和硫元素的定性检验
(1)将以下装置进行连接以完成实验(夹持仪器已略去,填接口字母代号)

a→
(2)将样品研磨成粉末的目的是
(3)确认样品中含有碳元素的现象是
Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量.称取样品m1g进行实验,充分反应后,测得C中生成的沉淀为m2g,该样品中碳的质量分数不小于
(5)乙同学认为,待一定量样品充分反应后,向E装置中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案是否合理?
(6)丙同学提议:为测定样品中硫的含量,可将c装置中试剂改为足量的30%双氧水,并按A→G→B→C装置连接进行实验,充分反应后,请你简述后续的实验方案
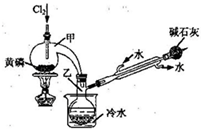 (2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
(2011?南京二模)PCl3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:| 熔点/℃ | 沸点/℃℃℃ | 密度/g?cm-3 | 其他 | |||||||||
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2
| ||||||||
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 | ||||||||
| POCl3 | 2 | 105 3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
①向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是
排尽装置中的空气,防止生成的PCl3与空气中的O2和H2O反应
排尽装置中的空气,防止生成的PCl3与空气中的O2和H2O反应
.②实验过程中,应控制
氯气的流量
氯气的流量
,以减少PCl5的生成.③蒸馏烧瓶乙中得到的粗产品含有POCl3、PCl5
等.加入黄磷加热除去PCl5后,通过
蒸馏
蒸馏
(填实验操作名称),即可得到PCl,纯品.(2)已知:
a.H3PO3+H2O+I2?H3PO4+2HI
b.(NH4)3BO3,溶液可与HI和H3PO4反应生成H3BO3
c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3=Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取mg产品,水解完全后在500mL容量瓶中定容;
步骤2:从容量瓶中移取25.00mL溶液置于碘量瓶中;
步骤3:准确加入c1mol?L-1碘溶液V1 mL(过量),再
迅速加入足量(NH4)3BO3溶液
迅速加入足量(NH4)3BO3溶液
;步骤4:
加入淀粉溶液,立即用Na2S2O3标准溶液回滴过量的碘
加入淀粉溶液,立即用Na2S2O3标准溶液回滴过量的碘
;滴至终点时消耗耗c2mol?L-1Na2S2O3溶液V2mL;②根据上述数据,该产品中PCl3的质量分数为2.75(c1v1-
| ||
| m |
2.75(c1v1-
| ||
| m |