摘要:H2S长期放置变浑浊或H2S不完全燃烧:
网址:http://m.1010jiajiao.com/timu3_id_158695[举报]
A、B、C均为常见的物质,且有如下转化关系:
(1)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子.
①请用离子方程式表示C溶液呈现酸碱性的原因:
②用石墨电极电解B的饱和溶液时,观察到的现象是
阳极反应式为
(2)若A、B、C均为含硫元素的物质,则A分子中的化学键类型是
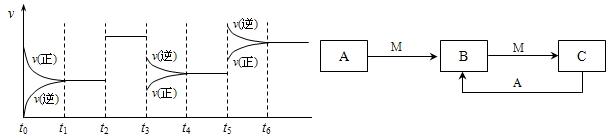
①若C在一定条件下可发生如下的反应:2SO2+O2 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
A t2时加入了催化剂 B t3时降低了温度
C t5时增大了压强 D t4~t5时间内反应物的转化率最低
②一定温度下的密闭容器内,充入4mol SO2、2mol O2 发生反应2SO2+O2 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
等温等容时再充入2mol SO2、1mol O2,达到平衡时若SO3的体积分数为b%,SO2的转化率为n,则a
查看习题详情和答案>>

(1)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子.
①请用离子方程式表示C溶液呈现酸碱性的原因:
HCO3-+H2O H2CO3+OH-
H2CO3+OH-
 H2CO3+OH-
H2CO3+OH-HCO3-+H2O H2CO3+OH-
H2CO3+OH-
. H2CO3+OH-
H2CO3+OH-②用石墨电极电解B的饱和溶液时,观察到的现象是
阴阳两极均有气体放出,溶液变浑浊或有晶体析出
阴阳两极均有气体放出,溶液变浑浊或有晶体析出
,阳极反应式为
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
,电解一段时间后,溶液的pH不变
不变
(填“增大”、“减小”或“不变”).(2)若A、B、C均为含硫元素的物质,则A分子中的化学键类型是
极性共价键
极性共价键
.①若C在一定条件下可发生如下的反应:2SO2+O2
 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是A
A
.A t2时加入了催化剂 B t3时降低了温度
C t5时增大了压强 D t4~t5时间内反应物的转化率最低
②一定温度下的密闭容器内,充入4mol SO2、2mol O2 发生反应2SO2+O2
 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m. 等温等容时再充入2mol SO2、1mol O2,达到平衡时若SO3的体积分数为b%,SO2的转化率为n,则a
<
<
b,m<
<
n(填“>”、“=”或“<”,下同).若改为等温等压,则a═
═
b,m═
═
n.下图每一方框中的字母代表一种反应物或生成物:
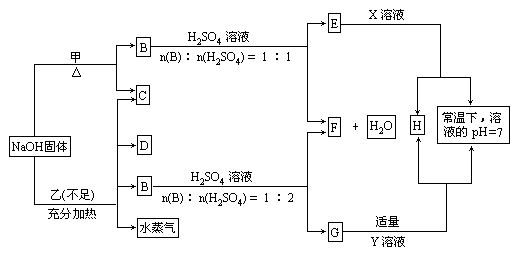
已知:常温下,C、D、F都是无色气体,其中C和D分子中的质子总数相等,C是一种可燃性气体,D能使湿润的红色石蕊试纸变蓝色,F能使澄清石灰水变浑浊;H是不溶于稀硝酸的白色沉淀.
(1)写出下列物质的化学式:C________、D________、甲________、X________.
(2)写出NaOH与乙反应的有关化学方程式:
_______________________________________
(3)写出G与Y反应后溶液为中性的离子方程式:
_______________________________________
查看习题详情和答案>>(2011?奉贤区一模)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关化学式前的系数及化学式填写在横线上.
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:(只要完成其中一项探究即可)
查看习题详情和答案>>
Ⅰ.测定过氧化的含量
请填写下列空白:
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL
容量瓶
容量瓶
(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关化学式前的系数及化学式填写在横线上.
2
2
MnO4-+5
5
H2O2+6
6
H+→2
2
Mn2++8
8
H2O+502
502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
.(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
| 0.085cV |
| ρ |
| 0.085cV |
| ρ |
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
偏高
偏高
(填“偏高”“偏低”“不变”).Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)
请将他们的实验方法和实验现象填入下表:(只要完成其中一项探究即可)
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 探究氧化性 | 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) |
产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) 产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) |
| 或探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) |
产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) 产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) |