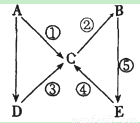
摘要:4.A.B.C.D.E是均含硫元素的五种物质.它们相互转化关系如图,
网址:http://m.1010jiajiao.com/timu3_id_158138[举报]
A、B、C、D、E是原子序数依次增大的五种短周期元素,A的某种核素不含中子,B、E同主族,且E的L层电子数是K层和M层电子数之和,C是所有短周期元素中半径最大的元素、C、D、E三种元素的最高价氧化物对应水化物两两之间均可反应.试解答下列问题:
(1)B元素的简单离子的结构示意简图为
 .
.
(2)A、D、E元素的名称分别为
(3)E元素在周期表中的位置是第
(4)五种元素的简单离子半径从大到小的顺序是
(5)五种元素中,得电子能力最强的是
查看习题详情和答案>>
(1)B元素的简单离子的结构示意简图为


(2)A、D、E元素的名称分别为
氢
氢
、硫
硫
、铝
铝
.(3)E元素在周期表中的位置是第
三
三
周期ⅥA
ⅥA
族.(4)五种元素的简单离子半径从大到小的顺序是
S2->O2->Na+>Al3+>H+
S2->O2->Na+>Al3+>H+
(用元素离子符号填写).(5)五种元素中,得电子能力最强的是
O
O
,失电子能力最强的是Na
Na
(填元素符号).A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,Y的用量最大.相关物质间的关系如图所示.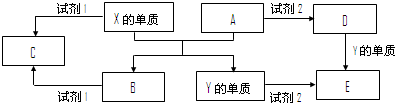
(1)X的单质与A反应的化学方程式是
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
②4.5克X的单质参加反应转移的电子数
(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
查看习题详情和答案>>

(1)X的单质与A反应的化学方程式是
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
.
| ||
(2)若试剂1是NaOH溶液,①X的单质与试剂1反应的离子方程式是
2Al+2H2O+2OH-═2AlO2-+3H2↑
2Al+2H2O+2OH-═2AlO2-+3H2↑
.②4.5克X的单质参加反应转移的电子数
3.01×1023
3.01×1023
.(3)若试剂1和试剂2均是稀硫酸.
①检验物质D的溶液中金属离子的方法是:
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+
.②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)
Al3++3H2O?Al(OH)3+3H+
Al3++3H2O?Al(OH)3+3H+
.③某高效净水剂是由Y(OH)SO4聚合得到的.工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
2FeSO4+2NaNO2+H2SO4═2Fe(OH)SO4+Na2SO4+2NO↑
.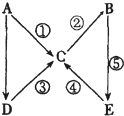 A、B、C、D、E五种物质均含有同一元素,且A为单质,有如图所示的转化关系.则下列判断不正确的是( )
A、B、C、D、E五种物质均含有同一元素,且A为单质,有如图所示的转化关系.则下列判断不正确的是( )| A、若ABCDE中同一元素的价态均不相同,则A为气态单质 | B、若A为金属钠,则由ImolD完全反应生成C时,一定有1mol电子转移 | C、若A为非金属硫,则④的反应类型既可以是氧化还原反应又可以是复分解反应 | D、若A为金属铁,则化合物C和D均可以由化合反应生成 |
 A、B、C、D、E五种中学常见物质均含有同一种元素,且A为单质,有如图所示的转化关系.则下列分析中不正确的是( )
A、B、C、D、E五种中学常见物质均含有同一种元素,且A为单质,有如图所示的转化关系.则下列分析中不正确的是( )