网址:http://m.1010jiajiao.com/timu3_id_157906[举报]
(20分)A物质是实验室一种无色有毒的挥发性液体,由X、Y两种短周期元素组成。A在空气中极易着火生成B气体和C气体;A不溶于水,但加热到423K可以和水反应,生成B气体和D气体,D只含两种元素,其中一种是Y。在交流放电的情况下,分解生成E气体、F固体两种物质,E物质和B化学式量几乎相等,含Y元素约72.7%;F是环状单质分子,具有冠状结构,易溶于A,F的式量约是C的4倍。E可在液氮条件下与HBr于77K生成含双键结构的物质G,冷却至室温可得G的环状三聚体H。
6-1 写出A、B、C、D、E、F、G、H的结构简式。
6-2 用X射线衍射法测得F的晶体为正交晶系,晶胞参数a=1048pm,b=1292pm,c=2455pm。已知该物质的密度为2.07g?cm-3。计算每个晶胞中F分子的数目。
6-3 自发现富勒烯以来,其神奇的结构和性能引起了人们对碳原子团簇广泛和深入的研究。除了碳原子团簇之外,其它元素的原子团簇是否也具有类似碳原子团簇的奇异的特性,这是个十分有趣的研究课题。F物质有很多同分异构体,在实验手段受到各种条件的限制时,理论研究是一种重要的补充。厦门大学化学系对F物质的原子团簇进行了理论计算,发现除了冠状结构外还有多种结构。其中一种X具有2次对称轴,以及两个包含对称轴的对称面,一配位和三配位原子数目相等;另外一种Y是一种椅式结构原子团簇增加2个原子形成,也具有二次对称轴,对称面和对称轴垂直。请画出这两种结构的原子团簇。
6-4 五氟化砷AsF5(2.93g)和上述物质F(0.37g)用四氮化四硫S4N4(0.53g)在液态SO2溶剂中发生完全的反应,溶剂和挥发性产物被泵抽出后得黄色固体残留物L(3.08g),分析J知其含有:As 28.04%,F 42.70%,N 5.25%,经分析L是离子化合物,阴离子为正八面体结构,阳离子为两种元素组成,结构是直线形。固体L(0.48g)溶于液态二氧化硫,和叠氮化铯Cs+N3-(0.31g)完全反应,收集应释放出得氮气于66.5kPa、298K为67.1cm3。反应混合物过滤得难溶蓝黑色纤维状固体J(0.16g)。分析J知其含有2种元素,其中含N 30.3%。红外光谱、X射线粉末衍射结果表明抽出SO2后残留物是六氟砷(V)酸铯。
(1)L的实验式是什么?
(2)提出L的结构式;
(3)写出配平的生成L的方程式;
(4)1mol L发生转化时生成氮气的物质的量;
(5)J的化学式;
(6)写出n mol L生成J的普遍离子方程式。
查看习题详情和答案>>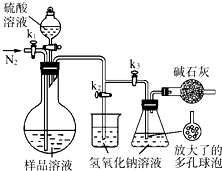 (2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
(2013?江苏三模)碳酸钠-过氧化氢加合物(aNa2CO3?bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:第1步:取适量碳酸钠溶解于一定量水中,倒入烧瓶中;再加入少量稳定剂(MgCl2和Na2SiO3),搅拌均匀.
第2步:将适量30%的H2O2溶液在搅拌状态下滴入烧瓶中,于15℃左右反应1h.
第3步:反应完毕后再加入适量无水乙醇,静置、结晶,过滤、干燥得产品.
(1)第1步中,稳定剂与水反应生成2种常见的难溶物,其化学方程式为
(2)第2步中,反应保持为15℃左右可采取的措施是
(3)第3步中,无水乙醇的作用是
(4)H2O2的含量可衡量产品的优劣.现称取m g(约0.5g)样品,用新煮沸过的蒸馏水配制成250mL溶液,取25.0mL于锥形瓶中,先用稀硫酸酸化,再用c mol?L-1 KMnO4溶液滴定至终点.
①配制250mL溶液所需的玻璃仪器有烧杯、玻璃棒、量筒、
②滴定终点观察到的现象是
(5)可模拟用蒸馏法测定样品中碳酸钠的含量.装置如图所示(加热和固定装置已略去),实验步骤如下:
步骤1:按右图所示组装仪器,检查装置气密性.
步骤2:准确量取(4)中所配溶液50mL于烧瓶中.
步骤3:准确量取40.00mL约0.2mol?NaOH溶液2份,分别注入烧杯和锥形瓶中.
步骤4:打开活塞k1、k2,关闭活塞k3,缓缓通入氮气一段时间后,关闭k1、k2,打开k3;经滴液漏斗向烧瓶中加入10mL 3mol?硫酸溶液.
步骤5:加热至烧瓶中的液体沸腾,蒸馏,并保持一段时间.
步骤6:经k1再缓缓通入氮气一段时间.
步骤7:向锥形瓶中加入酸碱指示剂,用c1 mol?H2SO4标准溶液滴定至终点,消耗H2SO4标准溶液V1 mL.
步骤8:将实验步骤1~7重复2次.
①步骤3中,准确移取40.00mL NaOH溶液所需要使用的仪器是
②步骤1~7中,确保生成的二氧化碳被氢氧化钠溶液完全吸收的实验步骤是
③为获得样品中碳酸钠的含量,还需补充的实验是
(14分)已知硫酸亚铁铵晶体为浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO 4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4?7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。
4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4?7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。
(已知: (NH4)2SO4+FeSO4+ 6H2O (NH4)2SO4?FeSO4?6H2O↓)根据下图回答:
(NH4)2SO4?FeSO4?6H2O↓)根据下图回答:
(1)步骤1中Na2CO3的主要作用是 。
(2)步骤2中铁屑过量的目的是(用离子方程式表示): 。步骤2中溶液趁热过滤的原因是 。
(3)步骤3中,加入(NH4)2SO4固体后,应加热到溶液表 面出现晶膜时,停止加热。为什么不能蒸干? 。需经过的实验操作包括: 、 、减压过滤(或抽滤)等得到较为干燥
面出现晶膜时,停止加热。为什么不能蒸干? 。需经过的实验操作包括: 、 、减压过滤(或抽滤)等得到较为干燥
的晶体。步骤3中制得的晶体要用无水乙醇洗涤的目的是 。
(4)摩尔盐产品中离子的检验:
甲同学提出可以用湿润的 试纸、稀盐酸和 溶液检验出这三种离子。
乙同学提出检验产品中的Fe2+,可以用KSCN溶液和另一种试剂 来检验,试简述乙同学操作和现象: 。
(5)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积10.00 mL。
①本实验的指示剂 。
| A.酚酞 | B.甲基橙 | C.石蕊 | D.不需要 |
③产品中Fe2+的质量分数为 。 查看习题详情和答案>>
 4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4?7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。
4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。以下是将绿矾(FeSO4?7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。(已知: (NH4)2SO4+FeSO4+ 6H2O
 (NH4)2SO4?FeSO4?6H2O↓)根据下图回答:
(NH4)2SO4?FeSO4?6H2O↓)根据下图回答: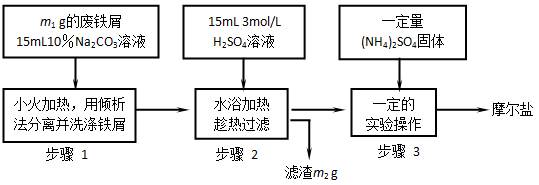
(1)步骤1中Na2CO3的主要作用是 。
(2)步骤2中铁屑过量的目的是(用离子方程式表示): 。步骤2中溶液趁热过滤的原因是 。

(3)步骤3中,加入(NH4)2SO4固体后,应加热到溶液表
 面出现晶膜时,停止加热。为什么不能蒸干? 。需经过的实验操作包括: 、 、减压过滤(或抽滤)等得到较为干燥
面出现晶膜时,停止加热。为什么不能蒸干? 。需经过的实验操作包括: 、 、减压过滤(或抽滤)等得到较为干燥的晶体。步骤3中制得的晶体要用无水乙醇洗涤的目的是 。
(4)摩尔盐产品中离子的检验:
甲同学提出可以用湿润的 试纸、稀盐酸和 溶液检验出这三种离子。
乙同学提出检验产品中的Fe2+,可以用KSCN溶液和另一种试剂 来检验,试简述乙同学操作和现象: 。
(5)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积10.00 mL。
①本实验的指示剂 。
| A.酚酞 | B.甲基橙 | C.石蕊 | D.不需要 |
③产品中Fe2+的质量分数为 。