网址:http://m.1010jiajiao.com/timu3_id_157194[举报]

(1)若A是一种两性氧化物,B的水溶液呈酸性,C的水溶液呈碱性,请写出A、B、C三种物质中含有的同一种金属元素的原子结构示意图
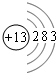

(2)若A为一种金属单质时,反应①②③均为化合反应,反应④为置换反应.请写出③可能的离子方程式
| ||
| ||
(3)若A、B、C是三种不同类别的固态物质,C是一种既含有离子键又含有共价键的化合物,溶于水电离出两种相同电子数的离子,B是工业上制取A、C的原料.实验室保存少量单质A的方法是
| ||
| ||
(4)若A、B均是可燃性物质,完全燃烧都生成气体C,常温下A溶液pH<7,将C通入A溶液中,pH值先增大后减小.
①将C通入如图2所示装置中,可以制得强电解质D的溶液,写出气体C发生的电极反应式
②该装置中H+的作用是
③若转移的电子数为6.02×1022时,左槽n(H+)的变化量为
(1)合成氨反应N2(g)+3H2(g)?2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡
(2)在25℃下,向浓度均为0.1mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出.
首先生成沉淀的离子方程式为
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)
(3)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应后溶液中
c(NH4+)=c(Cl-).则溶液显
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(o2)=
(1)合成氨反应N2(g)+3H2(g)?2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”).
(2)在25℃下,向浓度均为0.1mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出.
首先生成沉淀的离子方程式为 氨水过量后,生成的沉淀会部分溶解,写出溶解沉淀的离子方程式 .
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)
(3)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应后溶液中
c(NH4+)=c(Cl-).则溶液显 性(填“酸”、“碱”或“中”),请用含a的代数式表示NH3?H2O的电离常数Kb= .
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(o2)= mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,再次达到平衡后,n(SO3)的取值范围为 . 查看习题详情和答案>>
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、 、
、 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是________和________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为________(填字母)。
A.Br- B.
C.CH3COO- D.
(3)将19.2 g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式:________________,若要将Cu完全溶解,至少加入H2SO4的物质的量是________。
(4)若用惰性电极电解C和D的混合溶液,溶质的物质的量均为0.1 mol,请在坐标系中画出通电后阴极析出固体的质量m与通过电子的物质的量n的关系。(标明纵坐标数值)
(5)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为______________________________。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是________和________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为________(填字母)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2 g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式:________________,若要将Cu完全溶解,至少加入H2SO4的物质的量是________。
(4)若用惰性电极电解C和D的混合溶液,溶质的物质的量均为0.1 mol,请在坐标系中画出通电后阴极析出固体的质量m与通过电子的物质的量n的关系。(标明纵坐标数值)
(5)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为______________________________。