摘要:26.卤族元素包括 等元素.卤族元素原子结构的共同点是 .不同点是 .其中氧化性最强的单质是 .试举出两个化学性质说明它是最活泼的非金属元素 . .
网址:http://m.1010jiajiao.com/timu3_id_157088[举报]
 卤族元素是典型的非金属元素,包括F、Cl、Br、I等.请回答下面有关问题
卤族元素是典型的非金属元素,包括F、Cl、Br、I等.请回答下面有关问题(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大 的顺序是
(2)Br原子的核外电子排布式为
(3)用价层电子对互斥理论判断BeCl2的构型为
(4)CCl4分子中碳原子的杂化方式为
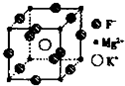
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为
卤族元素包括F、Cl、Br等.
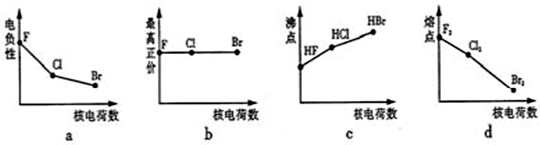
(1)下面曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 .
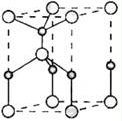
(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,如图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,该功能陶瓷的化学式为 .
(3)BCl3和NCl3中心原子的杂化方式分别为 和 .第一电离能介于B、N之间的第二周期元素有 种.
(4)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对电子的原子是 .
查看习题详情和答案>>
(1)下面曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是

(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,如图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为

(3)BCl3和NCl3中心原子的杂化方式分别为
(4)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对电子的原子是
卤族元素是典型的非金属元素,包括F、Cl、Br、I等。请回答下面有关问题
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是_____。
(2)Br原子的核外电子排布式为_________。
(3)用价层电子对互斥理论判断BeCl2的构型为________,BF3分子中B-F键的键角为________。
(4)CCl4分子中碳原子的杂化方式为________,NF3分子的空间构型为________。
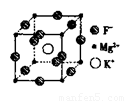
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为________。
查看习题详情和答案>>
卤族元素包括F、Cl、Br等。
(1)下列曲线表示卤族元素某种性质随核电荷数的变化趋势,正确的是 。

(2)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为 ,该功能陶瓷的化学式为 。
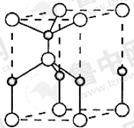
(3)BCl3和NCl3中心原子的杂化方式分别为 和 。第一电离能介于B、N之间的第二周期元素有 种。
(4)若BCl3与XYn通过B原子与X原子间的配位键结合形成配合物,则该配合物中提供孤对电子的原子是 。
查看习题详情和答案>>
卤族元素是典型的非金属元素,包括F、Cl、Br、I等。请回答下列问题:
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是
__________________。
(2)不同卤素原子之间可形成卤素互化物,如IBr,BrI3,BrF5,IF7等。其中卤素互化物中的化学键类型
为________。
(3)用价层电子对互斥理论判断BeCl2的构型为____________,BF3分子中B-F键的键角为____________。
(4)CCl4分子中的C原子和NF3分子中的N原子杂化方式是否相同?_____________。如果杂化相同,则其杂化方式为___________;如果杂化不同,则CCl4分子的C原子杂化方式为___________,NF3分子中N原子杂化方式为____________。
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中Mg 元素的质量分数为_________。
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是
__________________。
(2)不同卤素原子之间可形成卤素互化物,如IBr,BrI3,BrF5,IF7等。其中卤素互化物中的化学键类型
为________。
(3)用价层电子对互斥理论判断BeCl2的构型为____________,BF3分子中B-F键的键角为____________。
(4)CCl4分子中的C原子和NF3分子中的N原子杂化方式是否相同?_____________。如果杂化相同,则其杂化方式为___________;如果杂化不同,则CCl4分子的C原子杂化方式为___________,NF3分子中N原子杂化方式为____________。
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中Mg 元素的质量分数为_________。
