网址:http://m.1010jiajiao.com/timu3_id_155952[举报]
恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应: 2A(g) + B(g) ![]() xC (g) + D(s) C500解质 。,10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。(1)x = (2)从反应开始到40s达平衡状态,A的平均反应速率为 (3)平衡时容器中B的体积分数为 (4)该温度下此反应的平衡常数表达式为 数值是 (5)下列各项能表示该反应达到平衡状态是 ks5u
xC (g) + D(s) C500解质 。,10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。(1)x = (2)从反应开始到40s达平衡状态,A的平均反应速率为 (3)平衡时容器中B的体积分数为 (4)该温度下此反应的平衡常数表达式为 数值是 (5)下列各项能表示该反应达到平衡状态是 ks5u
A.消耗A的物质的量与生成D的物质的量之比为2∶1 B.容器中A、B的物质的量 n(A)∶n(B) =2∶1
C.气体的平均相对分子质量不再变化 D.压强不再变化 E.气体密度不再变化
(6)在相同温度下,若起始时c(A)=5 mol·L-1,c(B)=6mol·L-1,反应进行一段时间后,测得A的浓度为3mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”)。
查看习题详情和答案>>尿素 [CO(NH2)2 ]是首个由无机物人工合成的有机物。
⑴工业上尿CO2和NH3,在一定条件下合成,其反应方程式为 。
⑵当氨碳比![]() =4,CO2的转化率随时间的变化关系如题图1所示.
=4,CO2的转化率随时间的变化关系如题图1所示.
①A点的逆反应速率v逆(CO2) ![]() 点的正反应速率为v正(CO2)(填“大于”、“小于”或“等于”)
点的正反应速率为v正(CO2)(填“大于”、“小于”或“等于”)
②NH3的平衡转化率为 。
⑶⑶⑶ 人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图2。
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应以此为 、 。
③点解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解)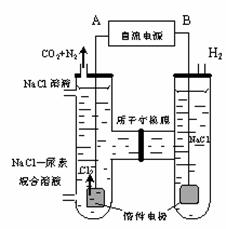 .
.
![]()
![]()
硫元素价态众多,可与卤素、氮等元素化合形成许多复杂化合物,在科学技术和生成中有重要的应用.根据题意完成下列计算:
(1)由硫与限量氯气在50~60°C反应16~20小时,可恰好完全反应,得到两种硫的氯化物A和B.A物质中的含硫量为0.131,B物质中的含氯量为0.816,A的相对分子质量比B大71.计算确定这两种氯化物的分子式分别为______.若上述反应得到的A、B的物质的量比为3:2,则参加反应的S和氯气的物质的量之比为______.
(2)硫的卤化物或卤氧化物都有强水解性,可以作脱水剂.SF4吸收V mL液态水(4℃),完全反应,得到3.2g SO2气体(假设SO2完全逸出)和10%的酸溶液,计算吸收的液态水的体积V为______mL.
(3)S4N4是亮橙色固体,不溶于水和有机溶剂,是一种重要的金属有机化学反应物.一般用S2Cl2、SCl2的惰性溶剂(CS2)氨解制得:6S2Cl2+16NH3→S4N4+S8+12NH4Cl;24SCl2+64NH3→4S4N4+S8+48NH4Cl.S2Cl2、SCl2的混合液体52.86g溶于足量的CS2中,再通入35.84L氨气(标准状况)完全氨解,产生14.080g硫单质.剩余氨气用40g水完全吸收形成氨水(密度为0.923g/mL).
计算:①该混合液体中S2Cl2、SCl2的物质的量之比为______.
②所得氨水的物质的量浓度为______(保留1位小数).
(4)S4N4与Ag在一定条件下反应,失去N2而缩合成(SN)x,(SN)x合成于1910年,过了五十年,才发现它在0.26K的低温下,可转变为超导体(superconductor).(SN)x的结构式如图:

已知1.20×105 mol S4N4与Ag发生缩合,失去了1.20×105 mol N2,生成二百聚物[(SN)200]和三百聚物.测得缩合产物中二百聚物的质量分数为0.50.
计算:①缩合产物中各缩合物的物质的量.
②若Ag的实际使用量为8.64kg,求Ag的循环使用次数.
查看习题详情和答案>>
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol A、2mol B | 6mol A、4mol B | 2mol C |
| 到达平衡的时间(min) | 5 | 8 | |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | w3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
| A、若x<4,则2c1<c2 |
| B、若w3=w1,可断定x=4 |
| C、无论x的值是多少,均有2ρ1=ρ2 |
| D、容器甲中反应从开始到达平衡平均速率为v(A)=0.3 mol?L-1?min-1 |