摘要:13.24.27 课时四:
网址:http://m.1010jiajiao.com/timu3_id_155866[举报]
摩尔盐[(NH4)2SO4?FeSO4?6H2O]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化.某实验小组查得硫酸铵、七水硫酸亚铁、硫酸亚铁铵的溶解度如表:
该实验小组在实验室按下列流程进行制取摩尔盐的实验:

(1)洗涤的目的是除去铁屑表面的
(2)反应Ⅰ为了加快铁屑(过量)的溶解,除了加热外,还可加入少量的
(3)蒸发浓缩前溶液中加入少量稀硫酸,其作用是:
(4)反应Ⅱ后的溶液经蒸发等操作所得固体用乙醇洗涤的目的是:
(5)在摩尔盐溶液中加入足量氨水,反应的离子方程式为:
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4?7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | - |
| (NH4)2SO4?FeSO4?6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |

(1)洗涤的目的是除去铁屑表面的
油污
油污
(填物质名称),用离子方程式表示碳酸钠溶液具有洗涤上述作用的原因CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
(2)反应Ⅰ为了加快铁屑(过量)的溶解,除了加热外,还可加入少量的
Cu或CuSO4
Cu或CuSO4
(填物质化学式),反应后Ⅰ要“趁热过滤”,其目的是:防止温度降低析出FeSO4?7H2O造成FeSO4的损失
防止温度降低析出FeSO4?7H2O造成FeSO4的损失
.(3)蒸发浓缩前溶液中加入少量稀硫酸,其作用是:
加入少量硫酸抑制Fe2+、NH4+的水解
加入少量硫酸抑制Fe2+、NH4+的水解
.(4)反应Ⅱ后的溶液经蒸发等操作所得固体用乙醇洗涤的目的是:
除去晶体表面的少量水分和其它可溶性杂质,避免水洗时晶体溶解损失
除去晶体表面的少量水分和其它可溶性杂质,避免水洗时晶体溶解损失
.(5)在摩尔盐溶液中加入足量氨水,反应的离子方程式为:
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
.摩尔盐[(NH4)2SO4?FeSO4?6H2O]是一种复盐,它易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,不易被氧化.某实验小组查得硫酸铵、七水硫酸亚铁、硫酸亚铁铵的溶解度如下表:
该实验小组在实验室按下列流程进行制取摩尔盐的实验:
(1)为了加快铁屑的溶解,可加入少量的
(2)反应Ⅰ进行后要“趁热过滤”,其目的是:
(3)反应Ⅱ后的溶液经蒸发等操作所得固体用乙醇洗涤的目的是:
(4)在摩尔盐溶液中加入足量氨水,反应的离子方程式为:
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| (NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
| FeSO4?7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | - |
| (NH4)2SO4?FeSO4?6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |

(1)为了加快铁屑的溶解,可加入少量的
铜或硫酸铜等
铜或硫酸铜等
(填物质名称).(2)反应Ⅰ进行后要“趁热过滤”,其目的是:
除去过量铁屑
除去过量铁屑
.实验中要在反应Ⅱ的溶液中加入少量稀硫酸,其作用是:防止温度降低析出FeSO4?7H2O造成FeSO4的损失,抑制Fe2+、NH4+的水解
防止温度降低析出FeSO4?7H2O造成FeSO4的损失,抑制Fe2+、NH4+的水解
.(3)反应Ⅱ后的溶液经蒸发等操作所得固体用乙醇洗涤的目的是:
除去晶体表面的少量水分
除去晶体表面的少量水分
.(4)在摩尔盐溶液中加入足量氨水,反应的离子方程式为:
Fe2++2(NH3?H2O)=Fe(OH)2↓+2NH4+
Fe2++2(NH3?H2O)=Fe(OH)2↓+2NH4+
.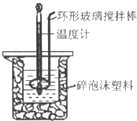 用50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热.
用50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热.
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指
(4)计算该实验发生中和反应时放出的热量为
(5)如果用50mL 0.55mol?L一的氨水(NH3?H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是