摘要:在标准状况下.50gCO和CO2的混合物的体积为33.6L.求这两种气体混合前的体积和质量各为多少? 附加题
网址:http://m.1010jiajiao.com/timu3_id_155250[举报]
(2012?武汉模拟)氢气的制取、储存和利用一直是化学领域的研究热点.

(1)H2O热分解可以得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图1所示.图1中
A、B表示的粒子依次是
(2)镍氢碱性电池已广泛应用于各种电器的供电,其中LaNi5有良好的储氢能力,其最大储氢量达到6.02
×1022个氢原子/cm3,则每立方厘米LaNi5吸附氢气的体积在标准状况下为
用固体LaNi5H6(各元素的化合价均可看作零)作负极反应物,该镍氢碱性电池放电时,负极电极反应式为
(3)有人设想利用H2实现碳循环,有关反应原理为:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0kJ/mol.一定温度下,在容积为1L的密闭容中,冲入1mol CO2和3molH2,测得CO2和 CH3OH(g)的浓度随时间的变化如图2所示.
①前10min CO2的平均反应速率为
②该温度下,此反应的平衡常数为
③为了提高CO2的平衡转化率可采取的措施是
A.升高温度
B.恒温恒容下再充入CO2
C.将CH3OH(g)从体系中分离出来
D.更换催化剂
E.恒温恒容下再充入 1mol CO2和3molH2.
查看习题详情和答案>>

(1)H2O热分解可以得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图1所示.图1中
A、B表示的粒子依次是
氢原子、氧原子
氢原子、氧原子
.A、B 重新生成水时的活化能=
=
0 (填“>”、“<”、或“=”);(2)镍氢碱性电池已广泛应用于各种电器的供电,其中LaNi5有良好的储氢能力,其最大储氢量达到6.02
×1022个氢原子/cm3,则每立方厘米LaNi5吸附氢气的体积在标准状况下为
1120
1120
mL;用固体LaNi5H6(各元素的化合价均可看作零)作负极反应物,该镍氢碱性电池放电时,负极电极反应式为
LaNi5H6+6OH--6e-═LaN5+6H2O
LaNi5H6+6OH--6e-═LaN5+6H2O
;(3)有人设想利用H2实现碳循环,有关反应原理为:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0kJ/mol.一定温度下,在容积为1L的密闭容中,冲入1mol CO2和3molH2,测得CO2和 CH3OH(g)的浓度随时间的变化如图2所示.
①前10min CO2的平均反应速率为
CO2
CO2
;②该温度下,此反应的平衡常数为
0.075mol/(L?min)
0.075mol/(L?min)
;③为了提高CO2的平衡转化率可采取的措施是
CE
CE
(填选项字母).A.升高温度
B.恒温恒容下再充入CO2
C.将CH3OH(g)从体系中分离出来
D.更换催化剂
E.恒温恒容下再充入 1mol CO2和3molH2.
已知随着硝酸浓度的不同,Fe与硝酸反应会生成NO或NO2;Fe 3+能与Fe发生下列反应:2Fe3++Fe═3Fe2+.现将某铁块与50g溶质的质量分数为63%的硝酸溶液发生反应,若反应中生成的气体均完全逸出并全部收集,请通过计算回答下列问题:
(1)若反应后,铁块全部溶解,硝酸仍有剩余,只收集到NO2气体,其体积在标准状况下为3.36L,则参加反应的Fe质量为
(2)若反应后,硝酸完全消耗,铁块仍有剩余,收集到的气体是NO2和NO的混合气体,其体积在标准状况下也为3.36L,则参加反应的Fe质量为
(3)若该铁块是表面含有Fe2O3的铁块,质量为 15g,且该铁块与上述硝酸恰好完全反应.如果将铁块中单质Fe的质量分数设为ω,则ω理论上的最大值是:
查看习题详情和答案>>
(1)若反应后,铁块全部溶解,硝酸仍有剩余,只收集到NO2气体,其体积在标准状况下为3.36L,则参加反应的Fe质量为
2.8
2.8
g.(2)若反应后,硝酸完全消耗,铁块仍有剩余,收集到的气体是NO2和NO的混合气体,其体积在标准状况下也为3.36L,则参加反应的Fe质量为
9.8
9.8
g.(3)若该铁块是表面含有Fe2O3的铁块,质量为 15g,且该铁块与上述硝酸恰好完全反应.如果将铁块中单质Fe的质量分数设为ω,则ω理论上的最大值是:
46.7%
46.7%
.(1)质量相等的两种物质SO2和SO3,两种物质中分子物质的量之比为
(2)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为
(3)在标准状况下,4.8g甲烷(CH4)所占的体积为
(4)中和浓度为4mol/L,体积为25mLH2SO4溶液,需要NaOH的质量为
查看习题详情和答案>>
5:4
5:4
,所含氧原子个数之比为5:6
5:6
.(2)20.6g NaR 含有Na+0.2mol,则NaR的摩尔质量为
103
103
g/mol,则含R 8.0g 的NaR的物质的量为0.1
0.1
mol.(3)在标准状况下,4.8g甲烷(CH4)所占的体积为
6.72
6.72
L,它与标准状况下13.44
13.44
L硫化氢(H2S)含有相同数目的氢原子.(4)中和浓度为4mol/L,体积为25mLH2SO4溶液,需要NaOH的质量为
8
8
g.现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
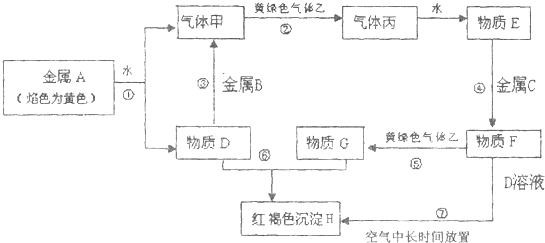
请根据以上信息回答下列问题:
(1)金属A、B、C分别是
(2)反应③的离子方程式为
(3)反应过程⑦涉及到的化学方程式
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成.该反应的化学方程式为
查看习题详情和答案>>

请根据以上信息回答下列问题:
(1)金属A、B、C分别是
Na
Na
、Al
Al
、Fe
Fe
.(2)反应③的离子方程式为
2Al+2OH-+2H2O=2AlO2-+3 H2↑
2Al+2OH-+2H2O=2AlO2-+3 H2↑
,在标准状况下测得,生成气体甲112mL,转移的电子数为0.01mol
0.01mol
.(3)反应过程⑦涉及到的化学方程式
FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3
FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成.该反应的化学方程式为
Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl
Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl
.