题目内容
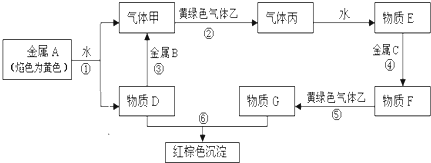
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
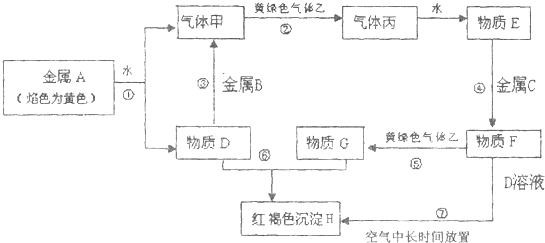
请根据以上信息回答下列问题:
(1)金属A、B、C分别是
(2)反应③的离子方程式为
(3)反应过程⑦涉及到的化学方程式
(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成.该反应的化学方程式为

请根据以上信息回答下列问题:
(1)金属A、B、C分别是
Na
Na
、Al
Al
、Fe
Fe
.(2)反应③的离子方程式为
2Al+2OH-+2H2O=2AlO2-+3 H2↑
2Al+2OH-+2H2O=2AlO2-+3 H2↑
,在标准状况下测得,生成气体甲112mL,转移的电子数为0.01mol
0.01mol
.(3)反应过程⑦涉及到的化学方程式
FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3
FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(4)向纯碱溶液中通入气体乙,可制得某种生产生活中常用的漂白、消毒的物质,同时有小苏打生成.该反应的化学方程式为
Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl
Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl
.分析:金属单质A的焰色反应为黄色,因此A为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,氯化氢溶于水生成元素,即E为盐酸,能与NaOH反应生成氢气的金属单质B为Al,红褐色沉淀H为Fe(OH)3,则金属单质C为Fe,F为FeCl2 ,G为FeCl3.结合对应物质的性质以及题目要求可解答该题.
解答:解:金属单质A的焰色反应为黄色,因此A为Na,与水反应生成的气体甲为H2,D为NaOH.黄绿色气体乙为Cl2,则丙为HCl.氯化氢溶于水生成元素,即E为盐酸,能与NaOH反应生成氢气的金属单质B为Al.红褐色沉淀H为Fe(OH)3,则金属单质C为Fe,F为FeCl2 ,G为FeCl3.
(1)由以上分析可知A为Na、B为Al、C为Al,故答案为:Na;Al; Fe;
(2)反应③为金属铝和氢氧化钠溶液反应,则反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2 ↑,在标准状况下测得,生成气体甲112mL,即生成0.005molH2,转移的电子数为0.005mol×2=0.01mol,
故答案为:2Al+2OH-+2H2O=2AlO2-+3 H2↑; 0.01mol;
(3)由于氢氧化亚铁极易被氧化生成氢氧化铁,所以若在F溶液中加入D溶液,并露置于空气中,能观察到的现象是先产生白色沉淀,然后沉淀变成灰绿色,最后变成红褐色,涉及反应的化学方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)向纯碱溶液中通入气体Cl2,可制得某种生产生活中常用的漂白、消毒的物质,应为NaClO,同时有小苏打生成,该反应的方程式为Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl,
故答案为:Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl.
(1)由以上分析可知A为Na、B为Al、C为Al,故答案为:Na;Al; Fe;
(2)反应③为金属铝和氢氧化钠溶液反应,则反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2 ↑,在标准状况下测得,生成气体甲112mL,即生成0.005molH2,转移的电子数为0.005mol×2=0.01mol,
故答案为:2Al+2OH-+2H2O=2AlO2-+3 H2↑; 0.01mol;
(3)由于氢氧化亚铁极易被氧化生成氢氧化铁,所以若在F溶液中加入D溶液,并露置于空气中,能观察到的现象是先产生白色沉淀,然后沉淀变成灰绿色,最后变成红褐色,涉及反应的化学方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)向纯碱溶液中通入气体Cl2,可制得某种生产生活中常用的漂白、消毒的物质,应为NaClO,同时有小苏打生成,该反应的方程式为Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl,
故答案为:Cl2+2Na2CO3+H2O=2NaHCO3+NaClO+NaCl.
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合.它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法.解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等.答题时注意体会、总结和积累,题目难度不大.

练习册系列答案
相关题目