摘要:B 解析:氢氧化钠溶液中加水.溶液任然显碱性.pH不会等于或小于7,NaOH溶液久置会与空气中的二氧化碳反应生成碳酸钠.所以加入盐酸后.盐酸先与氢氧化钠反应.再与碳酸钠反应产生二氧化碳气体.
网址:http://m.1010jiajiao.com/timu3_id_15498[举报]
水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)为了防止水的污染,下列做法中,有利于保护水资源的是 (填序号).
①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(2)从组成角度看:水是由 组成的.
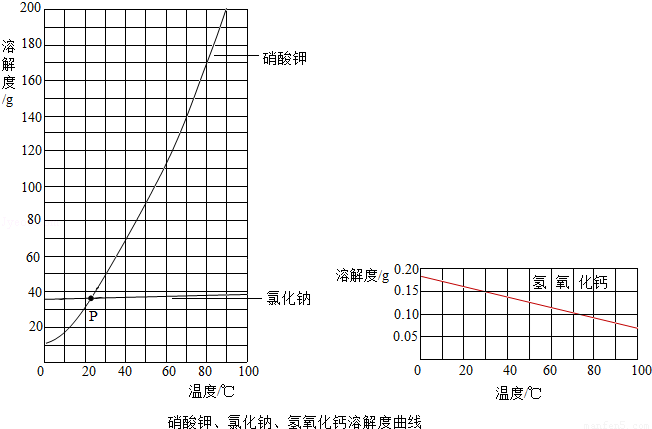
(3)根据上图,回答问题.
①交点P的含义是 .
②随温度升高,氢氧化钙溶解度的变化趋势是 .
③如下图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中,若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解.
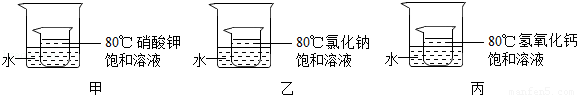
下列关于该实验的说法中,正确的是 (填字母序号).
A.甲、乙的小烧杯中有晶体析出,丙的小烧杯中变浑浊
B.整个过程中,三只小烧杯中溶剂的质量不变
C.80℃时,硝酸钾溶液的浓度一定大于氯化钠溶液的浓度
D.整个过程中,三种物质的溶液均为饱和溶液.
查看习题详情和答案>>
水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)为了防止水的污染,下列做法中,有利于保护水资源的是 (填序号).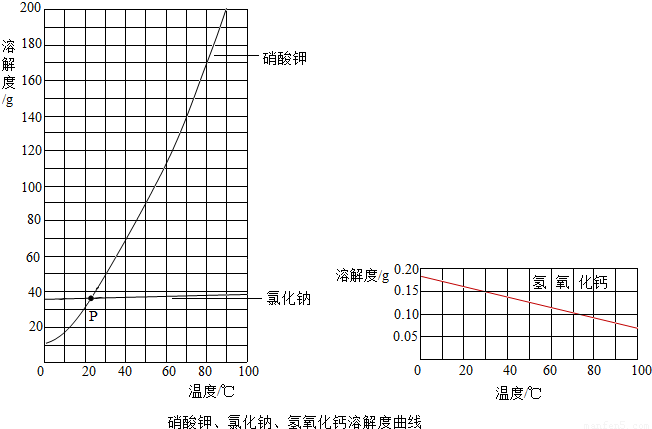
①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(2)从组成角度看:水是由 组成的.
(3)根据上图,回答问题.
①交点P的含义是 .
②随温度升高,氢氧化钙溶解度的变化趋势是 .
③如下图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中,若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解.
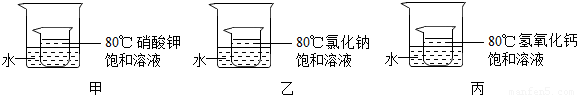
下列关于该实验的说法中,正确的是 (填字母序号).
A.甲、乙的小烧杯中有晶体析出,丙的小烧杯中变浑浊
B.整个过程中,三只小烧杯中溶剂的质量不变
C.80℃时,硝酸钾溶液的浓度一定大于氯化钠溶液的浓度
D.整个过程中,三种物质的溶液均为饱和溶液. 查看习题详情和答案>>
(1)为了防止水的污染,下列做法中,有利于保护水资源的是 (填序号).

①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(2)从组成角度看:水是由 组成的.
(3)根据上图,回答问题.
①交点P的含义是 .
②随温度升高,氢氧化钙溶解度的变化趋势是 .
③如下图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中,若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解.

下列关于该实验的说法中,正确的是 (填字母序号).
A.甲、乙的小烧杯中有晶体析出,丙的小烧杯中变浑浊
B.整个过程中,三只小烧杯中溶剂的质量不变
C.80℃时,硝酸钾溶液的浓度一定大于氯化钠溶液的浓度
D.整个过程中,三种物质的溶液均为饱和溶液. 查看习题详情和答案>>
水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)为了防止水的污染,下列做法中,有利于保护水资源的是 (填序号).
①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(2)从组成角度看:水是由 组成的.
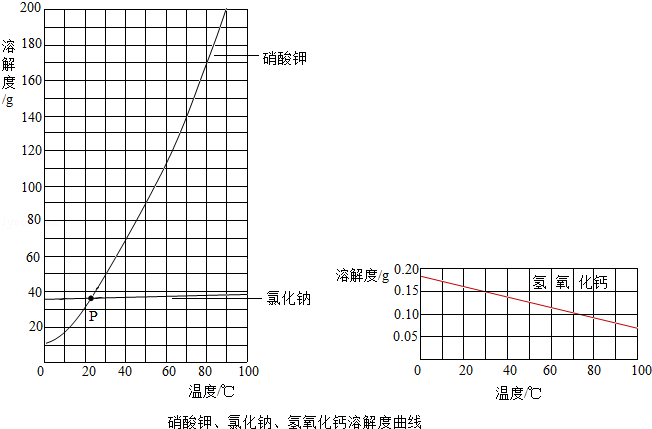
(3)根据上图,回答问题.
①交点P的含义是 .
②随温度升高,氢氧化钙溶解度的变化趋势是 .
③如下图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中,若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解.

下列关于该实验的说法中,正确的是 (填字母序号).
(1)为了防止水的污染,下列做法中,有利于保护水资源的是 (填序号).

①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放.
(2)从组成角度看:水是由 组成的.
(3)根据上图,回答问题.
①交点P的含义是 .
②随温度升高,氢氧化钙溶解度的变化趋势是 .
③如下图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中,若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解.

下列关于该实验的说法中,正确的是 (填字母序号).
| A.甲、乙的小烧杯中有晶体析出,丙的小烧杯中变浑浊 |
| B.整个过程中,三只小烧杯中溶剂的质量不变 |
| C.80℃时,硝酸钾溶液的浓度一定大于氯化钠溶液的浓度 |
| D.整个过程中,三种物质的溶液均为饱和溶液. |
叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究.
[查阅资料]
①NaN3受撞击会生成Na、N2.
②NaN3遇盐酸、H2SO4溶液无气体生成.
③碱石灰是CaO和 NaOH的混合物.
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和氨气(NH3).
[问题探究]
(1)汽车经撞击后,30毫秒内引发NaN3迅速分解,写出该反应的化学方程式:
(2)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示):
(3)为测定某工业级NaN3样品中含有Na2CO3的质量分数,化学小组同学设计了如下实验装置.
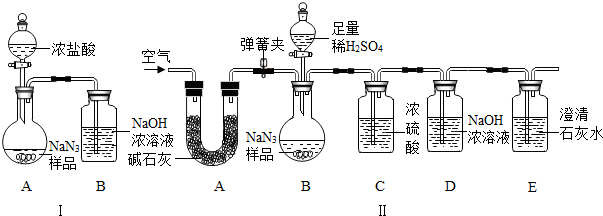
①小明同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是
②小刚同学在大家讨论的基础上,设计了装置II.请分析:装置II中A的作用
③根据装置II,小组同学设计的实验步骤有:
a.称量装置D.
b.称量样品,检查装置气密性.
c.打开弹簧夹,鼓入空气.
d.打开分液漏斗的活塞和玻璃塞,注入足量的稀硫酸,关闭活塞和玻璃塞.
其正确顺序为
(4)该小组对某一工业级NaN3样品进行检测.取100克该样品于烧杯中,加水将其溶解,然后逐滴加入一定溶质质量分数的稀硫酸并不断振荡.
首先发生的反应是:2Na2CO3+H2SO4=2NaHCO3+Na2SO4;
然后发生的反应是:2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑;
在上述过程中生成二氧化碳的质量与加入稀硫酸质量的关系如图甲所示.

①请你根据以上信息,在图乙的坐标系中画出检测过程中烧杯中溶液的质量随滴加硫酸溶液质量的变化曲线.
②计算该样品中纯碱的质量分数.
查看习题详情和答案>>
[查阅资料]
①NaN3受撞击会生成Na、N2.
②NaN3遇盐酸、H2SO4溶液无气体生成.
③碱石灰是CaO和 NaOH的混合物.
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和氨气(NH3).
[问题探究]
(1)汽车经撞击后,30毫秒内引发NaN3迅速分解,写出该反应的化学方程式:
2NaN3
2Na+3N2↑
| ||
2NaN3
2Na+3N2↑
.
| ||
(2)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示):
2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.(3)为测定某工业级NaN3样品中含有Na2CO3的质量分数,化学小组同学设计了如下实验装置.

①小明同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是
浓盐酸有挥发性,挥发出的氯化氢气体会带来实验误差
浓盐酸有挥发性,挥发出的氯化氢气体会带来实验误差
.②小刚同学在大家讨论的基础上,设计了装置II.请分析:装置II中A的作用
吸收空气中的二氧化碳和水
吸收空气中的二氧化碳和水
;若无装置C,对测定结果造成的影响是偏大
偏大
(填“偏大”、“偏小”或“无影响”);③根据装置II,小组同学设计的实验步骤有:
a.称量装置D.
b.称量样品,检查装置气密性.
c.打开弹簧夹,鼓入空气.
d.打开分液漏斗的活塞和玻璃塞,注入足量的稀硫酸,关闭活塞和玻璃塞.
其正确顺序为
bcadca
bcadca
(填字母序号,可重复).(4)该小组对某一工业级NaN3样品进行检测.取100克该样品于烧杯中,加水将其溶解,然后逐滴加入一定溶质质量分数的稀硫酸并不断振荡.
首先发生的反应是:2Na2CO3+H2SO4=2NaHCO3+Na2SO4;
然后发生的反应是:2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑;
在上述过程中生成二氧化碳的质量与加入稀硫酸质量的关系如图甲所示.

①请你根据以上信息,在图乙的坐标系中画出检测过程中烧杯中溶液的质量随滴加硫酸溶液质量的变化曲线.
②计算该样品中纯碱的质量分数.
KNO3、NaCl溶液在生产、生活中起着十分重要的作用.下表是它们在不同温度时的溶解度,如图一是它们的溶解度曲线.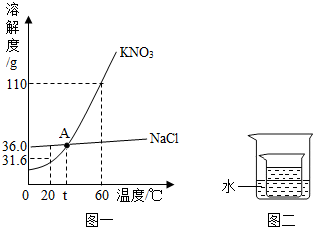
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.8 |
(2)30℃时,KNO3的溶解度是______g.
(3)图中A点的含义是______.
(4)某同学做了如下两个实验.实验1:20℃时,100g水
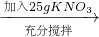 a
a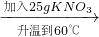
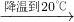 c
c实验2:20℃时,100g水
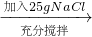 d
d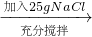 e
e f
f判断a~f对应的溶液中,为饱和溶液的是______;
由实验1、2可知,使不饱和溶液转化为饱和溶液的方法有______.
(5)如图二所示,小烧杯中盛放的是实验1中的KNO3溶液b.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是______(填字母).
A.冰 B.氧化钙 C.硝酸铵 D.干冰 E固体氢氧化钠. 查看习题详情和答案>>