摘要:操作:取洁净铂丝(或无锈铁丝或镍.铬.钨丝)在盐酸中浸洗后灼烧至无色.然后蘸取待测物灼烧.
网址:http://m.1010jiajiao.com/timu3_id_154407[举报]
下列实验操作或描述中正确的是(填写字母) .
A.用托盘天平称取5.85g氯化钠固体
B.提取碘水中的碘单质时,可选用酒精作萃取剂
C.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
D.观察钾元素焰色反应的操作是:将铂丝在稀盐酸中洗涤后直接蘸取固体氯化钾,置于酒精灯火焰上进行灼烧,根据火焰是否显紫色来确定
E.氧化铁与足量盐酸反应后的溶液中滴加硫氰化钾溶液会生成血红色沉淀. 查看习题详情和答案>>
A.用托盘天平称取5.85g氯化钠固体
B.提取碘水中的碘单质时,可选用酒精作萃取剂
C.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
D.观察钾元素焰色反应的操作是:将铂丝在稀盐酸中洗涤后直接蘸取固体氯化钾,置于酒精灯火焰上进行灼烧,根据火焰是否显紫色来确定
E.氧化铁与足量盐酸反应后的溶液中滴加硫氰化钾溶液会生成血红色沉淀. 查看习题详情和答案>>
以下为中学常见物质,转化关系如下.C与B溶液反应产生气体F,D可在F中燃烧,图中部分产物略去.
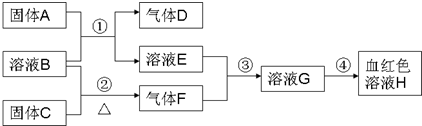
(1)写出固体C化学式
(2)实验室用①制取D、B溶液应为
(3)如何检验E中的阳离子
(4)实验室配制G溶液,操作为
(5)除③可实现E→G外,请用其他物质实现E→G,化学方程式
(6)4gD在空气中完全燃烧生成液体物质时,放出热量为QkJ,写出该反应的热化学方程式
查看习题详情和答案>>

(1)写出固体C化学式
MnO2
MnO2
.(2)实验室用①制取D、B溶液应为
稀
稀
溶液(“浓”或“稀”);若用②制取F,B溶液应为浓
浓
溶液(“浓”或“稀”).写出②反应方程式MnO2+4HCl
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl
MnCl2+Cl2↑+2H2O
.
| ||
(3)如何检验E中的阳离子
取少许溶液E与试管中,滴加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变为红色,说明含有Fe2+
取少许溶液E与试管中,滴加KSCN溶液,溶液不变红色,再滴加新制氯水,溶液变为红色,说明含有Fe2+
.(4)实验室配制G溶液,操作为
将氯化铁溶解在盐酸中,再稀释到所需要的浓度
将氯化铁溶解在盐酸中,再稀释到所需要的浓度
.(5)除③可实现E→G外,请用其他物质实现E→G,化学方程式
2FeCl2+H2O2+2HCl=2FeCl3+2H2O
2FeCl2+H2O2+2HCl=2FeCl3+2H2O
.(6)4gD在空气中完全燃烧生成液体物质时,放出热量为QkJ,写出该反应的热化学方程式
2H2(g)+O2(g)=2H2O(l);△H=-QkJ/mol
2H2(g)+O2(g)=2H2O(l);△H=-QkJ/mol
.下列离子检验的操作与现象不正确的是
A.向少许待测液中滴加KSCN溶液无明显变化,再滴入氯水,溶液呈红色,则待测液中含有Fe2+
B.向少许待测液中滴几滴稀硝酸,再滴加少许硝酸银,有白色沉淀生成,则待测液中含有Cl-
C.向少许待测液中逐滴加入稀氨水至过量,产生白色胶状沉淀,后又逐渐溶解,则待测液中含有Al3+
D.用洁净的铂丝用盐酸清洗后在酒精灯外焰上灼烧至无色时蘸取待测液在外焰上灼烧,透过蓝色钴玻璃观察火焰为紫色,则待测液中含有K+
查看习题详情和答案>>
下列实验现象和结论相符的是
操作及现象 结论
A 某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 溶液中一定含有CO32-
B 某溶液中加入硝酸银,产生白色沉淀 溶液中一定含有Cl-
C 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 溶液中有Na+,无K+
D 向某溶液中先加几滴KSCN溶液,无明显现象,再滴氯水,溶液变红 溶液中一定含有Fe2+
查看习题详情和答案>>
下列离子检验的操作与现象不正确的是
| A.向少许待测液中滴加KSCN溶液无明显变化,再滴入氯水,溶液呈红色,则待测液中含有Fe2+ |
| B.向少许待测液中滴几滴稀硝酸,再滴加少许硝酸银,有白色沉淀生成,则待测液中含有Cl- |
| C.向少许待测液中逐滴加入稀氨水至过量,产生白色胶状沉淀,后又逐渐溶解,则待测液中含有Al3+ |
| D.用洁净的铂丝用盐酸清洗后在酒精灯外焰上灼烧至无色时蘸取待测液在外焰上灼烧,透过蓝色钴玻璃观察火焰为紫色,则待测液中含有K+ |