摘要:pH与溶液酸.碱性的关系 pH=7.溶液呈中性 pH<7.溶液呈酸性 pH>7.溶液呈碱性 注意:(1)pH越小.酸性越强.当酸溶液被稀释时.溶液pH变大.但不会变成碱性.所以稀释后溶液的pH不会大于7.反之.pH越大.碱性越强.当碱溶液稀释时.溶液pH变小.但不会变成酸性.所以稀释后溶液的pH不会小于7. (2)并不是所有的盐溶液pH都等于7.如NaCl.K2SO4 等溶液.pH=7.而Na2CO3溶液pH>7.
网址:http://m.1010jiajiao.com/timu3_id_15440[举报]
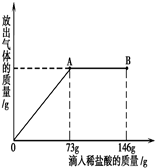
 已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中A点时,烧杯中溶液pH
=
=
7(填>、=、<);至图中B点时,溶液中的溶质为NaCl和HCl
NaCl和HCl
(填化学式).(2)求原混合物中氯化钠的质量分数.
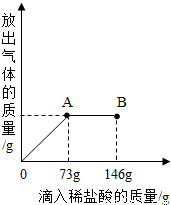
已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物。向其中逐渐滴加溶质质量分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)
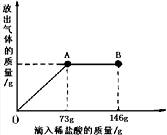
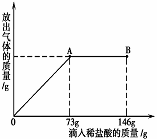
已知Na2CO3的水溶液呈碱性,在一烧杯中盛有31.4g Na2CO3溶液,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如右图所示,请根据题意回答问题:
(1) 当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7
(填“>”、“=”或“<”);
(2) 原溶液中碳酸钠的质量;
(3) 当滴加稀盐酸至图中A点时,通过计算求出其中溶质的质量分数(计算结果精确到0.1%)。
 |
查看习题详情和答案>>