摘要:加热1.218g晶体RCl2.xH2O.使之失去全部结晶水得到0.570gRCl2.把这些RCl2溶解于水配成200ml溶液.取出100ml溶液正好与40ml 0.15mol/lAgNO3溶液完全反应.则 (1) R是什么元素? (2) x的数值是多少?
网址:http://m.1010jiajiao.com/timu3_id_154167[举报]
(2013?江苏二模)硫酸亚铁铵(NH4)2Fe(SO4)2?6H2O是一种浅绿色晶体,在水中的溶解度较小,不溶于乙醇.某实验小组利用镀锌铁片来制备硫酸亚铁铵的过程如下:
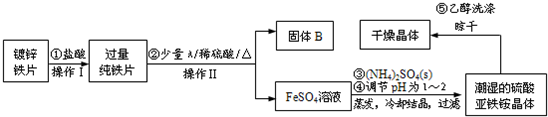
(1)加入盐酸是为了除去锌镀层,判断锌镀层已被除去的现象是
(2)A物质可以是
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
加入少量A物质的目的是
(3)操作Ⅱ的名称为
(4)采用晾干而不用加热烘干晶体的原因是
(5)工业上常用K2Cr2O7溶液测定硫酸亚铁铵的纯度,反应中Cr2O72-被还原成Cr3+.
写出硫酸亚铁铵溶液与酸性K2Cr2O7溶液反应的离子方程式
查看习题详情和答案>>

(1)加入盐酸是为了除去锌镀层,判断锌镀层已被除去的现象是
反应速率突然减小(或铁片表面生成的气泡突然减少,意思相近均给分)
反应速率突然减小(或铁片表面生成的气泡突然减少,意思相近均给分)
.(2)A物质可以是
bd
bd
(选填序号).a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
加入少量A物质的目的是
加快铁与稀硫酸的反应速率
加快铁与稀硫酸的反应速率
.(3)操作Ⅱ的名称为
过滤
过滤
.(4)采用晾干而不用加热烘干晶体的原因是
避免加热过程中晶体受热分解失去结晶水或被空气氧化
避免加热过程中晶体受热分解失去结晶水或被空气氧化
.(5)工业上常用K2Cr2O7溶液测定硫酸亚铁铵的纯度,反应中Cr2O72-被还原成Cr3+.
写出硫酸亚铁铵溶液与酸性K2Cr2O7溶液反应的离子方程式
6Fe2++Cr2O72-+14H+=2Cr3++6Fe3++7H2O
6Fe2++Cr2O72-+14H+=2Cr3++6Fe3++7H2O
.常温时,已知:I2+2S2
=S4
+2I-.相关物质的溶度积常数见下表:
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2?2H2O晶体,加入
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是Cu2+发生水解反应.由CuCl2?2H2O晶体得到纯的无水CuCl2的合理方法是
(3)某学习小组用“间接碘量法”测定含有CuCl2?2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成CuI(2Cu2++4I-=2CuI↓+I2)白色沉淀.用0.1000mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用
②该试样中CuCl2?2H2O的质量百分数为
查看习题详情和答案>>
| O | 2- 3 |
| O | 2- 6 |
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
Cu(OH)2或Cu2(OH)2CO3
Cu(OH)2或Cu2(OH)2CO3
,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L
2.6×10-9mol/L
.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2?2H2O晶体.(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是Cu2+发生水解反应.由CuCl2?2H2O晶体得到纯的无水CuCl2的合理方法是
在干燥的HCl气流中加热脱水;
在干燥的HCl气流中加热脱水;
.(3)某学习小组用“间接碘量法”测定含有CuCl2?2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成CuI(2Cu2++4I-=2CuI↓+I2)白色沉淀.用0.1000mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用
淀粉溶液;
淀粉溶液;
作滴定指示剂,滴定终点的现象是蓝色褪去,放置一定时间后不恢复原色;
蓝色褪去,放置一定时间后不恢复原色;
.②该试样中CuCl2?2H2O的质量百分数为
95%
95%
.硫代硫酸钠是一种常见的化工原料.将SO2通入按一定比例配成的Na2S和Na2CO3的混合溶液中,便可得到Na2S2O3,其制备反应方程式为:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
(1)在配制混合溶液前先将蒸馏水加热煮沸一段时间后待用,其目的是 .
(2)用该方法获得的Na2S2O3.H2O晶体中常混有一定量的杂质.某兴趣小组欲对其中所含杂质成分进行探究(不考虑副反应和杂质所带的结晶水).
[提出假设]
假设1:晶体中只含Na2CO3杂质
假设2:晶体中只含Na2S杂质
假设3:
[查阅资料]
①SO2+2H2S═3S↓+2H2O
②Na2S2O3在中性、碱性溶液中较稳定,而在酸性溶液中能迅速反应:
Na2S2O3+H2SO4═Na2SO4+S↑+SO2↑+H2O
③CuSO4+H2S=CuS↓(黑色)+H2SO4
[判断与思考]
某同学取少量制得的晶体溶于足量稀H2SO4,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此认为假设2不成立.你认为其结论是否合理? (填“合理”、“不合理”)并说明理由:
[设计方案进行实验]
基于假设1,完成下表实验方案、现象及结论(仪器自选).
限选实验试剂:3mol?L-1H2SO4、1mol?L-1NaOH、酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
(3)已知:2Na2S2O3+I2═2NaI+Na2S4O6.为测定所制得晶体的纯度,该小组以淀粉作指示剂,
用0.010mol?L-1的碘水进行多次取样滴定,测得Na2S2O3?5H2O的含量约为102%.若所用试剂及操作均无不当,产生该结果最可能的原因是 .
查看习题详情和答案>>
(1)在配制混合溶液前先将蒸馏水加热煮沸一段时间后待用,其目的是
(2)用该方法获得的Na2S2O3.H2O晶体中常混有一定量的杂质.某兴趣小组欲对其中所含杂质成分进行探究(不考虑副反应和杂质所带的结晶水).
[提出假设]
假设1:晶体中只含Na2CO3杂质
假设2:晶体中只含Na2S杂质
假设3:
[查阅资料]
①SO2+2H2S═3S↓+2H2O
②Na2S2O3在中性、碱性溶液中较稳定,而在酸性溶液中能迅速反应:
Na2S2O3+H2SO4═Na2SO4+S↑+SO2↑+H2O
③CuSO4+H2S=CuS↓(黑色)+H2SO4
[判断与思考]
某同学取少量制得的晶体溶于足量稀H2SO4,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此认为假设2不成立.你认为其结论是否合理?
[设计方案进行实验]
基于假设1,完成下表实验方案、现象及结论(仪器自选).
限选实验试剂:3mol?L-1H2SO4、1mol?L-1NaOH、酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
| 实验方案 | 现象及结论 |
用0.010mol?L-1的碘水进行多次取样滴定,测得Na2S2O3?5H2O的含量约为102%.若所用试剂及操作均无不当,产生该结果最可能的原因是
(2011?四川)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,在110℃可完全失去结晶水.为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+.向反应后的溶液中计入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL滴定中MnO4-被还原成Mn2+.
重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液19.98mL
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作步骤依次是:称量、
②加入锌粉的目的是
③写出步骤三中发生反应的离子方程式
④实验测得该晶体中铁的质量分数为
(2)结晶水的测定
加热晶体,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,至于空气中冷却,称量并记录质量;计算结晶水含量.请纠正实验过程中的两处错误;
查看习题详情和答案>>
(1)铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+.向反应后的溶液中计入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL滴定中MnO4-被还原成Mn2+.
重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液19.98mL
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作步骤依次是:称量、
溶解
溶解
、转移、洗涤并转移、定容
定容
摇匀.②加入锌粉的目的是
将Fe3+恰好还原成Fe2+
将Fe3+恰好还原成Fe2+
.③写出步骤三中发生反应的离子方程式
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
.④实验测得该晶体中铁的质量分数为
11.2%
11.2%
.在步骤二中,若加入的KMnO4的溶液的量不够,则测得的铁含量偏高
偏高
.(选填“偏低”“偏高”“不变”)(2)结晶水的测定
加热晶体,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至110℃,恒温一段时间,至于空气中冷却,称量并记录质量;计算结晶水含量.请纠正实验过程中的两处错误;
加热后的晶体要在干燥器中冷却
加热后的晶体要在干燥器中冷却
;两次称量质量差不超过0.1g
两次称量质量差不超过0.1g
.用电解方法制取金属镁时需要用无水MgCl2,而直接加热MgCl2WH2O晶体却得 不到无水MgCl2.某化学小组利用如图1实验装置(夹持装置已略去),通过测定反应物及生成物的质量来确定MgCl2.6H2O晶体受热分解的产物.请回答:

(1)按气流方向连接各装置,其顺序为 (填仪器接口字母编号).
(2)实验过程中,装置B中的CCl4层始终为无色.装置B的作用为 .实验结束后,需通入一段儿时间的空气,其目的为
(3)实验中称取8.12g MgCl2?6H20晶体,充分反应后,装置A中残留固体质量为3.06g,装置B增重1.46g,装置C增重3.60g.则装置A中发生反应的化学方程式为
(4)直接加热MgCl2?WH2O晶体得不到无水MgCl2的原因为 .
(5)某同学采用图2装置(夹持装置已略去)由MgCl2?6H2O晶体制得了无水MgCl2.
①方框中所缺装置从图1A、B、C、D中选择,按气流方向连接依次为 (只填仪器字母编号,不必填接口顺序)
②圆底烧瓶中盛装的液体甲为 .
查看习题详情和答案>>

(1)按气流方向连接各装置,其顺序为
(2)实验过程中,装置B中的CCl4层始终为无色.装置B的作用为
(3)实验中称取8.12g MgCl2?6H20晶体,充分反应后,装置A中残留固体质量为3.06g,装置B增重1.46g,装置C增重3.60g.则装置A中发生反应的化学方程式为
(4)直接加热MgCl2?WH2O晶体得不到无水MgCl2的原因为
(5)某同学采用图2装置(夹持装置已略去)由MgCl2?6H2O晶体制得了无水MgCl2.
①方框中所缺装置从图1A、B、C、D中选择,按气流方向连接依次为
②圆底烧瓶中盛装的液体甲为