网址:http://m.1010jiajiao.com/timu3_id_153412[举报]
(1)若该反应在常温下能剧烈发生,C、D中有一种物质的溶液能腐蚀玻璃,则反应的化学方程式可表示为________________
(2)若A、C、D均含有氧元素,且这三种物质混合后能形成一种新物质E,B与E能发生化合反应生成盐F,则F中含有的化学键类型有____________,F中阴、阳离子的电子数之比为________________。
(3)若A为固体,B为碱溶液,C与D在酸性条件下又能转化为A,则A与B反应的离子方程式为________________________。
(4)若A、B、C均为固体,D为气体。写出两个满足此条件的化学方程式:____________、 ____________
已知A、B、C、D分别是由短周期元素组成的四种微粒,它们之间有如图所示的转化关系,且A是一种含有18电子的微粒,C是一种含有10电子的微粒。请回答下列
问题:
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程式:_____________________________________________________。
(2)若B、D属于同主族元素形成的单质分子,写出C的化学式:________。
(3)若A、B均是含有2个原子核的微粒,且B中含有10个电子,D中含有18个电子,则A、B之间发生反应的离子方程式为_____________________。
(4)若D是一种含有22电子的分子,则符合如图所示转化关系的A为__________(写出物质的化学式,如果是有机物则写出相应的结构简式)。
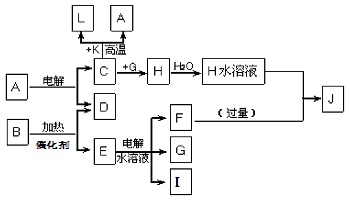
(1)工业上制C用A不用H的原因_________________
(2)写出C与K反应的化学方程式 ____________,该反应的反应物总能量__________(填“大于”或“小于”)生成物总能量
(3)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,接通电源(短时间)电解E水溶液的化学方程式______________________,电解后为使溶液与电解前完全相同,需向上述溶液中通入______________
(4)J与H反应的离子方程式为___________________,若在上述转化关系中每一步反应均为恰好反应,且不考虑C+K→A+L的变化时,为了最终得到J,则A、B的物质的量之比为
____________
已知:A、B、D为中学化学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol丁分子中不同原子的数目比为1∶2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如下图所示(某些条件已略去).

请回答:
(1)单质A的组成元素在周期表中的位置是________.
(2)乙中所包含的化学键类型有________(填字母序号).
a.离子键
b.极性共价键
c.非极性共价键
(3)用电子式表示丙分子的形成过程________.
(4)反应①的化学方程式为________.
(5)丁的电子式为________.
(6)反应②中,0.5 mol NaClO参加反应时,转移1 mol电子,其离子方程式为:________.
(7)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分.已知该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为________.