摘要:有一无色透明晶体是高熔点.高硬度的物质.A在纯氧中不能燃烧.但在高温时既能与大理石又能与纯碱反应.都放出气体B,A不能溶于强酸但能溶于氢氟酸.A与烧碱溶液反应生成C的水溶液.B通入C的溶液时.生成不稳定的白色胶状沉淀.在干燥的空气中.失去部分水.得白色粉末D.D加热又生成A.则: A .B .C .D .
网址:http://m.1010jiajiao.com/timu3_id_152786[举报]
有一天然透明晶体A是高熔点,高硬度的物质,A在纯氧中不能燃烧,但在高温时既能和石灰石,又能和纯碱反应都放出气体B,A虽不能溶于强酸,但却能溶于氢氟酸,并生成气体C,A和烧碱溶液反应生成D的水溶液,当气体B通入溶液中去,能生成不稳定的白色胶状沉淀E,在干燥的空气中,E失去部分水,得到白色粉末F,F加热后重新生成A。
(1)试推断出A、B、C、D、E、F各是什么物质?写出其化学式。
(2)写出有关反应的化学方程式。
查看习题详情和答案>>今有一无色透明溶液,只可能含有以下离子中的若干中:K+、H+、Mg2+、Fe3+、Ba2+、SO42-、CO32-、NO3-,现取二份各100mL溶液进行如下实验:
①第一份加足量NaHCO3溶液加热后,收集到气体0.04mol
②第二份加足量Ba(NO3)2 溶液充分反应后过滤干燥,得沉淀4.66g.
根据上述实验回答
(1)溶液中一定不存在的离子是
(2)溶液中可能存在的离子是
(3)写出①发生反应的离子方程式
(4)写出②发生反应的离子方程式
查看习题详情和答案>>
①第一份加足量NaHCO3溶液加热后,收集到气体0.04mol
②第二份加足量Ba(NO3)2 溶液充分反应后过滤干燥,得沉淀4.66g.
根据上述实验回答
(1)溶液中一定不存在的离子是
Fe3+、Ba2+、CO32-
Fe3+、Ba2+、CO32-
;(2)溶液中可能存在的离子是
K+、Mg2+
K+、Mg2+
;(3)写出①发生反应的离子方程式
HCO3-+H+=CO2↑+H2O
HCO3-+H+=CO2↑+H2O
;(4)写出②发生反应的离子方程式
Ba2++SO42-=BaSO4↓
Ba2++SO42-=BaSO4↓
.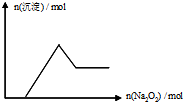 有一无色透明溶液,取出少量滴入BaCl2溶液,只有白色沉淀生成;另取一定体积的无色溶液加入过量Na2O2,有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示,根据以上判断在 ①H+②NH4+;③Al3+④Mg2+⑤Fe2+⑥NO3-⑦SO42-⑧CO32-中一定存在的离子是( )
有一无色透明溶液,取出少量滴入BaCl2溶液,只有白色沉淀生成;另取一定体积的无色溶液加入过量Na2O2,有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示,根据以上判断在 ①H+②NH4+;③Al3+④Mg2+⑤Fe2+⑥NO3-⑦SO42-⑧CO32-中一定存在的离子是( )
查看习题详情和答案>>
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液的实验如下:
由此判断:
(1)溶液中一定存在的离子是
(2)写出(3)步的离子方程式:
(3)写出(5)步沉淀部分溶解的离子方程式:
查看习题详情和答案>>
| 实验步骤 | 实验现象 | (1)取少量该溶液,加几滴甲基橙 | 溶液变红色 | (2)取少量该溶液加热浓缩,加Cu片和浓硫酸,加热 | 有无色气体产生,气体遇空气可以变成红棕色 | (3)取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 | (4)取(3)中的上层清夜,加AgNO3 | 有稳定的白色沉淀生成,且不溶于稀硝酸 | (5)取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
(1)溶液中一定存在的离子是
NO3-、SO42-、Mg2+、Al3+
NO3-、SO42-、Mg2+、Al3+
;溶液中肯定不存在的离子是:I-、Ba2+、Fe2+、HCO3-
I-、Ba2+、Fe2+、HCO3-
.(2)写出(3)步的离子方程式:
SO42-+Ba2+=BaSO4↓
SO42-+Ba2+=BaSO4↓
.(3)写出(5)步沉淀部分溶解的离子方程式:
Al(OH)3+OH-=[Al(OH)4]-
Al(OH)3+OH-=[Al(OH)4]-
.有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
(1)溶液中肯定存在的离子是 .
(2)溶液中肯定不存在的离子是 .
(3)为进一步确定其他离子,应该补充的实验是 .
查看习题详情和答案>>
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴甲基橙 | 溶液变红色 |
| ②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,后在空气中又变成红棕色 |
| ③取少量该溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ⑤取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(2)溶液中肯定不存在的离子是
(3)为进一步确定其他离子,应该补充的实验是