摘要: CBDA ,CDAB ,CADB ,CBDA
网址:http://m.1010jiajiao.com/timu3_id_151149[举报]
(2013?德州一模)海水是应用前景广阔的化工原料资源,从海水中可提取各种化工原料.如图1是工业 上对海水的几项综合利用的示意图(已知气体X为电解饱和食盐水所得;母液苦卤中主要 含有Ca2+、Mg2+,Cl-,SO42?、Br-等离子)请回答: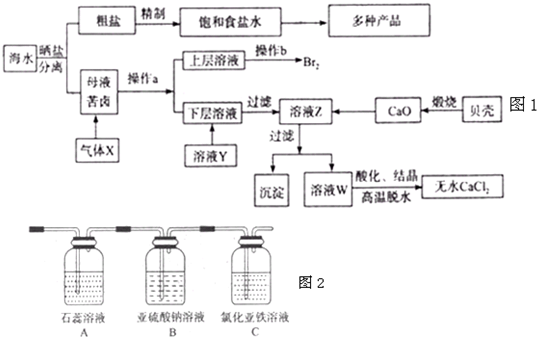
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,梢制时所用的试剂为:A.盐酸B.氯化钡溶 液C.氢氧化钠溶液D.碳酸钠溶液,则加入试剂的顺序是(填编号)
(2)气体X的化学式为
(3)加入溶液Y的目的是
(4)将气体X依次通过如图2所示装置以验证气体X的性质:
①通入气体X后,A中出现的现象是
②C装置中发生反应的离子方程式为
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤)
查看习题详情和答案>>

(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,梢制时所用的试剂为:A.盐酸B.氯化钡溶 液C.氢氧化钠溶液D.碳酸钠溶液,则加入试剂的顺序是(填编号)
BDCA 或 CBDA 或BCDA等
BDCA 或 CBDA 或BCDA等
.(2)气体X的化学式为
Cl2
Cl2
,操作a所用的主要仪器是分液漏斗
分液漏斗
.(3)加入溶液Y的目的是
除去溶液中的SO42-
除去溶液中的SO42-
,用CaO调节溶液Z的pH,可以除去Mg2+得到溶液W.由表中数据可知,理论上可选择pH最大范围是11.0≤pH<12.2
11.0≤pH<12.2
.酸化溶液W时,使用的试剂为盐酸
盐酸
.| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
①通入气体X后,A中出现的现象是
溶液先变红,后褪色;
溶液先变红,后褪色;
.②C装置中发生反应的离子方程式为
2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
.③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤)
取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化.
取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化.
.新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图1所示.
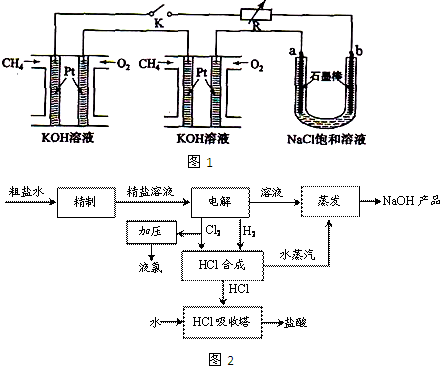
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)闭合K开关后,a、b电极上均有气体产生.电解氯化钠溶液的总反应方程式为
(3)氯碱厂电解饱和食盐水制取烧碱,同时制盐酸的工艺流程如图2:
根据题意完成下列填空:
①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A 盐酸;B BaCl2溶液;C NaOH溶液;D Na2CO3溶液.加入试剂的顺序是
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
③HCl合成反应中保持过量的气体是
④利用HCl合成时放出的热量来产生水蒸汽,用于NaOH溶液的蒸发,这样做的优点是
⑤检验NaOH产品中是否含有NaCl的实验方案是
查看习题详情和答案>>

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
2O2+4H2O+8e-=8OH-
2O2+4H2O+8e-=8OH-
、CH4+10OH--8e-=CO32-+7H2O
CH4+10OH--8e-=CO32-+7H2O
.(2)闭合K开关后,a、b电极上均有气体产生.电解氯化钠溶液的总反应方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
;
| ||
(3)氯碱厂电解饱和食盐水制取烧碱,同时制盐酸的工艺流程如图2:
根据题意完成下列填空:
①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A 盐酸;B BaCl2溶液;C NaOH溶液;D Na2CO3溶液.加入试剂的顺序是
BCDA或CBDA
BCDA或CBDA
.②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
2Cl--2e→Cl2
2Cl--2e→Cl2
.与电源负极线连的电极附近溶液pH变大
变大
(变大、不变、变小).③HCl合成反应中保持过量的气体是
氢气
氢气
;从HCl合成塔的观察口能观察到的现象是苍白色火焰
苍白色火焰
.④利用HCl合成时放出的热量来产生水蒸汽,用于NaOH溶液的蒸发,这样做的优点是
充分利用能量
充分利用能量
.⑤检验NaOH产品中是否含有NaCl的实验方案是
加足量稀硝酸至呈酸性,然后滴加硝酸银溶液,若产生白色沉淀,则含有氯化钠
加足量稀硝酸至呈酸性,然后滴加硝酸银溶液,若产生白色沉淀,则含有氯化钠
.海水是应用前景广阔的化工原料资源,从海水中可提取各种化工原料.如图是工业上对海水的几项综合利用的示意图:
回答下列问题:
(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A:盐酸;B:BaCl2溶液;C:NaOH溶液;D:Na2CO3溶液.加入试剂的顺序是
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱.
①气体A、B是CO2或NH3,则气体A应是
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品
NH4Cl晶体,则通入NH3的作用是
(3)空气吹出法工艺,是目前“海水提溴”的最主要方法之一.
a、写出步骤①④反应的离子方程式:①
b、在步骤⑥的蒸馏过程中,温度应控制在80-90℃、温度过高过低都不利于生产,请解释原因:
c、在步骤①、②之后并未直接用“含溴的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是
查看习题详情和答案>>

回答下列问题:
(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A:盐酸;B:BaCl2溶液;C:NaOH溶液;D:Na2CO3溶液.加入试剂的顺序是
CBDA或BCDA
CBDA或BCDA
.②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
,与电源负极线连的电极附近溶液pH变大
变大
(变大、不变、变小).(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱.
①气体A、B是CO2或NH3,则气体A应是
NH3
NH3
(填化学式).C的制得发生反应的化学方程式为2NaHCO3
Na2CO3+CO2↑+H2O
| ||
2NaHCO3
Na2CO3+CO2↑+H2O
.
| ||
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品
NH4Cl晶体,则通入NH3的作用是
氨气溶于水后生成氨水,氨水电离成铵根和氢氧根离子,增大铵根的浓度有利于氯化铵的析出来,溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度;
氨气溶于水后生成氨水,氨水电离成铵根和氢氧根离子,增大铵根的浓度有利于氯化铵的析出来,溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度;
.(3)空气吹出法工艺,是目前“海水提溴”的最主要方法之一.
a、写出步骤①④反应的离子方程式:①
2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
;④SO2+Br2+2H2O=2HBr+H2SO4
SO2+Br2+2H2O=2HBr+H2SO4
.b、在步骤⑥的蒸馏过程中,温度应控制在80-90℃、温度过高过低都不利于生产,请解释原因:
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
.c、在步骤①、②之后并未直接用“含溴的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是
“空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低.
“空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低.
.我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务.
(1)海水中所含元素质量最大的是
(2)①从海水中提取粗盐采用的方法是
②工业上常以食盐为原料制备氯气,再用氯气制备漂白粉,用化学方程式表示工业上制漂白粉的原理
(3)提取NaCl后剩余的海水(母液)中,可用来提取Mg和Br2.
①如用来提取Mg,请完成具体工业流程(注:( )内填所需试剂,【】内填操作)
②根据上述提取镁的全过程,没有涉及到的反应类型是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
③若用来提取Br2,用离子方程式表示提取溴的原理:
④方法A:母液提取Mg后,再用来提取Br2;方法B:母液提取Br2后,再用来提取Mg.哪个更合适
查看习题详情和答案>>
(1)海水中所含元素质量最大的是
O
O
(写元素符号),被称作海洋元素的是Br
Br
(写元素符号).(2)①从海水中提取粗盐采用的方法是
蒸发结晶
蒸发结晶
,粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为A盐酸、B氯化钡溶液、C氢氧化钠溶液、D碳酸钠溶液,以上试剂添加的顺序为CBDA(其它合理答案即可)
CBDA(其它合理答案即可)
.②工业上常以食盐为原料制备氯气,再用氯气制备漂白粉,用化学方程式表示工业上制漂白粉的原理
Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O
Cl2+Ca(OH)2=Ca2++Cl-+ClO-+H2O
(3)提取NaCl后剩余的海水(母液)中,可用来提取Mg和Br2.
①如用来提取Mg,请完成具体工业流程(注:( )内填所需试剂,【】内填操作)

②根据上述提取镁的全过程,没有涉及到的反应类型是
C
C
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
③若用来提取Br2,用离子方程式表示提取溴的原理:
Cl2+2Br-=2Cl-+Br2
Cl2+2Br-=2Cl-+Br2
.④方法A:母液提取Mg后,再用来提取Br2;方法B:母液提取Br2后,再用来提取Mg.哪个更合适
B
B
(填“A”或“B”),你的理由是若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
.海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:

请回答:
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液.
则加入试剂的顺序是(填编号)
(2)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是
A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
(3)写出电解饱和NaCl溶液的离子反应方程式:
(4)此工业煅烧贝壳得到氧化钙.石灰石和贝壳的主要成份相同,事实上,石灰石在许多化学工业生产都发挥了极大的作用,请写出一条化工生产中碳酸钙参与的化学反应方程式(此工业涉及的方程式除外)
(5)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是
(6)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
查看习题详情和答案>>

请回答:
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液.
则加入试剂的顺序是(填编号)
BDCA 或 CBDA 或BCDA等
BDCA 或 CBDA 或BCDA等
.(2)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是
D
D
.A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
(3)写出电解饱和NaCl溶液的离子反应方程式:
2Cl-+2H2O
Cl2↑+H2↑+2OH-
| ||
2Cl-+2H2O
Cl2↑+H2↑+2OH-
.
| ||
(4)此工业煅烧贝壳得到氧化钙.石灰石和贝壳的主要成份相同,事实上,石灰石在许多化学工业生产都发挥了极大的作用,请写出一条化工生产中碳酸钙参与的化学反应方程式(此工业涉及的方程式除外)
CaCO3+SiO2
CaSiO3+CO2↑
| ||
CaCO3+SiO2
CaSiO3+CO2↑
.
| ||
(5)利用MgCl2?6H2O可制得无水氯化镁,应采取的措施是
在HCl气流中加热脱水(防止MgCl2水解)
在HCl气流中加热脱水(防止MgCl2水解)
.(6)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
H2O+Na2SO3+Br2═Na2SO4+2HBr
H2O+Na2SO3+Br2═Na2SO4+2HBr
.