摘要: A.B.C.D.E是钠及其化合物.有以下反应: ① 2A B + CO2↑+ H2O ② A + C ===== B + H2O ③ 2D + 2H2O ===== 4C + O2↑ ④ 2D + 2CO2 ===== 2B + O2 ⑤ B + Ca(OH)2 ===== 2C + CaCO3↓ ⑥ 2E + 2H2O ===== 2 C + H2↑ 试推断:A ,B ,C ,D , E .
网址:http://m.1010jiajiao.com/timu3_id_151132[举报]
A、B、C、F是中学化学常见的单质,在相同条件下,气体A的密度大于气体B的密度,其有关转化如下:
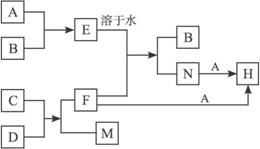
(1)写出有关反应的离子方程式:
E的水溶液+F:_______________________________________________________。
A+N:_______________________________________________________________。
M对应的氢氧化物与氢氧化钠溶液反应:_________________________________。
C+D:(写出化学方程式)______________________________________________。
(2)在足量的稀N溶液中,加入少量A的水溶液,振荡后溶液变为黄绿色。甲同学认为这不是发生化学反应所致,是A水溶液的颜色,乙同学认为这是发生化学反应所致,使溶液变黄绿色的物质是生成物和A水溶液的混合颜色。
①请你判断哪位同学的推断是正确的?_____________(填“甲”或“乙”)。
②请你设计一个实验探究你的判断(要求写出化学实验必要的操作步骤,所用化学试剂及实验现象,以及得出的化学实验结论)。
查看习题详情和答案>>短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示.请回答下列问题:
(1)B、C、D元素的非金属性由大到小的顺序为
(2)E的氢化物与其最高价氧化物对应水化物的钾盐共热能发生反应,生成一种气体单质.反应的化学方程式为
(3)C有多种氧化物,其中甲的相对分子质量最小,在一定条件下2L甲气体与0.5L氧气相混合,若该气体混合物被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是
(4)在298K下,A、B的单质各1mol 完全燃烧,分别放出热量aKJ和bKJ,又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来.若此置换反应生成3mol B的单质,则该反应在298K下的△H
(5)要证明与D同主族且相邻的元素的非金属性与E的非金属性强弱,正确、合理的实验操作及现象是
查看习题详情和答案>>
| B | C | D | ||
| A | E |
O>N>C
O>N>C
;(填元素符号)(2)E的氢化物与其最高价氧化物对应水化物的钾盐共热能发生反应,生成一种气体单质.反应的化学方程式为
8HCl+KClO4
KCl+4Cl2↑+4H2O
| ||
8HCl+KClO4
KCl+4Cl2↑+4H2O
;
| ||
(3)C有多种氧化物,其中甲的相对分子质量最小,在一定条件下2L甲气体与0.5L氧气相混合,若该气体混合物被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是
NaNO2
NaNO2
;(4)在298K下,A、B的单质各1mol 完全燃烧,分别放出热量aKJ和bKJ,又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来.若此置换反应生成3mol B的单质,则该反应在298K下的△H
-(4a-3b)KJ/mol
-(4a-3b)KJ/mol
(注:题中所设单质的为稳定单质).(5)要证明与D同主族且相邻的元素的非金属性与E的非金属性强弱,正确、合理的实验操作及现象是
将氯气(或氯水)滴入硫化钠溶液中,有淡黄色沉淀生成
将氯气(或氯水)滴入硫化钠溶液中,有淡黄色沉淀生成
.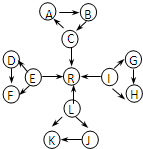 元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):
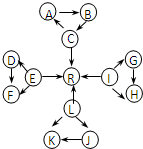
元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):已知:
①图中每个小三角形的三种物质中至少含有一种相同元素,A与B、D与F、K与J均由2种相同的元素组成.
②C、E、L、I为常见固体单质,C、E、L都能与水在一定条件下反应生成气体单质R,D、F中所含的非金属元素所形成的单质常温下为黄绿色气体.其余物质为常见化合物.
③K为淡黄色固体.
④C、L、I三元素原子的原子序数之和为30.
根据以上信息,回答下列问题:
(1)写出R的名称
氢气
氢气
,K的电子式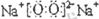
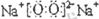
(2)请些出由B生成C的化学反应方程式
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(3)I和氢氧化钠溶液反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;I和氢氧化钠溶液反应除生成R还可以得到H.请用离子方程式表示H水溶液呈碱性的原因:AlO2-+2H2O?Al(OH)3+OH-
AlO2-+2H2O?Al(OH)3+OH-
.(4)用惰性电极电解一定浓度足量的L的氯化物水溶液,若电解结束时,通过电子为0.2mol,电解后恢复至室温,溶液的体积为2L,则溶液的pH为
13
13
.(5)若D溶液中含有杂质F,如何除去?
若D为FeCl2,则通入足量的Cl2即可.若D为FeCl3,则加入足量的Fe,再过滤
若D为FeCl2,则通入足量的Cl2即可.若D为FeCl3,则加入足量的Fe,再过滤
.已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示[部分产物略去,Fe能与足量稀HNO3反应生成Fe(NO3)3]。下列说法错误的是 ( )。
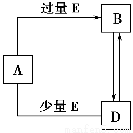
A.A、B、D可能是钠及其化合物
B.A、B、D可能是铁及其化合物
C.A、B、D可能是铝及其化合物
D.A、B、D不可能是非金属及其化合物
查看习题详情和答案>>
 元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):
元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):