摘要:17.(1)有K+.Ar.Cl-三种微粒,其中最难失去电子的是 . (2)右图为周期表中短周期的一部分.B.C两元素的核外电 子数之和等于A的质量数的2倍, A原子核内质子数和中子数相等,则 A为 ; B为 ;C为 ; (3)由两核10个电子组成的化合物为 ,由五核10个电子组成的化合物 为 ,由11个质子和10个电子组成的微粒有 .
网址:http://m.1010jiajiao.com/timu3_id_151093[举报]
将KCl和CrCl3两种固体混合物共熔,得化合物X.X由K、Cr、Cl三种元素组成.将1.892gX中的铬元素全部氧化成Cr2O72-,后者可以从过量的KI溶液中氧化出2.667g碘单质(Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O).向溶有1.892gX的溶液中加入过量AgNO3溶液,可得到4.52g AgCl沉淀.则X的化学式为( )
查看习题详情和答案>>
将KCl和CrCl3两种固体混合,共熔化合,制得化合物X,X是由K、Cr、Cl三种元素组成,将1.892gX中的Cr元素全部氧化成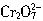 ,这些
,这些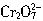 可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为:
可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为:
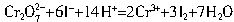
如果取溶有1.892gX的溶液,加入过量的AgNO3溶液,可以得到AgCl沉淀4.52g,则表示X组成的化学式为( )。
A.K3Cr2Cl9 B.K3Cr2Cl7
C.K3Cr2Cl5 D.K2CrCl4 查看习题详情和答案>>
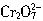 ,这些
,这些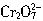 可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为:
可以从过量的KI溶液中氧化出2.667gI2,反应的离子方程式为: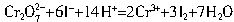
如果取溶有1.892gX的溶液,加入过量的AgNO3溶液,可以得到AgCl沉淀4.52g,则表示X组成的化学式为( )。
A.K3Cr2Cl9 B.K3Cr2Cl7
C.K3Cr2Cl5 D.K2CrCl4 查看习题详情和答案>>
将KCl和CrCl3两种固体混合,共熔化合,制得化合物X,X是由K、Cr、Cl三种元素组成,将1.892g X中的Cr元素全部氧化成Cr2O72-,这些Cr2O72可以从过量的KI溶液中氧化生成2.667g碘单质,反应的离子方程式为:Cr2O72-+6I-+14H+![]() 2Cr3++3I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3溶液,可以得到AgCl沉淀4.52g,则X的化学式为
2Cr3++3I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3溶液,可以得到AgCl沉淀4.52g,则X的化学式为
A.K3Cr2Cl9 B.K3Cr2Cl7 C.K3Cr2Cl5 D.K2CrCl4
查看习题详情和答案>>