网址:http://m.1010jiajiao.com/timu3_id_151038[举报]
下列两题分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,请你选择其中一题作答,如果两题全做,则按A题评分。
A.(12分)【物质结构与性质】
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
⑴科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ・mol-1) | 786 | 715 | 3 401 |
4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是 ▲ 。
⑵科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示。

①写出基态Cu原子的核外电子排布式 ▲ ;金属铜采用下列 ▲ (填字母代号)堆积方式。
 |
A B C D
②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来) ▲ 。
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响 ▲ 。
④SO42-的空间构型是 ▲ 。
B.(12分)【实验化学】
硫酸亚铁铵的化学式为(NH4)2SO4・FeSO4・6H2O,又名莫尔盐,是分析化学中常见的还原剂。某化学研究小组设计如下实验来制备莫尔盐并测定硫酸亚铁铵的纯度。
步骤一:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入Na2CO3溶液,加热,过滤、洗涤、干燥、称量,质量记为m1。
步骤二:FeSO4的制备。将上述铁屑加入到一定量的稀H2SO4中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量记为m2。
步骤三:硫酸亚铁铵的制备。准确称取所需质量的(NH4)2SO4加入“步骤二”中的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥,称量所得晶体质量。
步骤四:用比色法测定硫酸亚铁铵的纯度。
 回答下列问题:
回答下列问题:
⑴步骤三中称取的(NH4)2SO4质量为 ▲ 。
⑵①铁屑用Na2CO3溶液处理的目的是 ▲ 。制备FeSO4溶液时,用右图装置趁热过滤,原因是 ▲ 。
②将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机是 ▲ 。
③比色法测定硫酸亚铁铵纯度的实验步骤为:Fe3+标准色阶的配制、待测硫酸亚铁铵溶液的配制、比色测定。标准色阶和待测液配制时除均需加入少量稀HCl溶液外,还应注意的问题是 ▲ 。
④该实验最终通过 ▲ 确定硫酸亚铁铵产品等级。
查看习题详情和答案>>| 序号 | 元素 | 结构及性质 | ||
| ① | A | A的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 | ||
| ② | B | B原子最外层电子数是内层电子总数的
| ||
| ③ | C | C的氧化物是两性氧化物,且作为耐火材料 | ||
| ④ | D | A、D、E组成的36电子的化合物甲是家用消毒剂的主要成分 | ||
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 | ||
| ⑥ | F | F元素最高正价与最低负价的代数和为4 |
(1)按A、B、C顺序,三种元素的金属性逐渐
(2)一定条件下,将4.0mol FE2和3.0mol E2 通入到体积为 2L的密闭容器中.反应达到平衡时,容器中为FE2 0.4mol,则此反应的平衡常数是.改变下列条件,能使平衡向正反应方向进行且平衡常数不变的是
a.增大压强 b.降低温度 c.使用催化剂 d.增大反应物的浓度
(3)E与氢元素可以形成原子个数比分别为1:2、1:1的两种化合物X和Y.
| 实验编号 | 温度/℃ | 加入试剂 | 加入Y的量 |
| ① | 5 | 2滴 1mol/L FeCl3溶液 | 4mL 10% 的Y溶液 |
| ② | 40 | 2滴1mol/L FeCl3溶液 | 4mL 10% 的Y溶液 |
| ③ | 40 | 2滴1mol/L FeCl3溶液 2mL X |
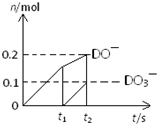
(4)一定量的石灰乳中通入一定量的D单质,两者恰好完全反应,生成物中有三种含D元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.则t2时刻消耗氢氧化钙质量为
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ?mol-1) | 786 | 715 | 3 401 |
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图1,其中配位键和氢键均采用虚线表示.
①写出基态Cu原子的核外电子排布式
金属铜采用图2中

②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响:
③SO42-的空间构型是
(3)下列哪个系列的排列顺序正好是电负性减小的顺序?
A.K、Na、Li B.O、Cl、H C.As、P、H D.三者都是.
(1)请参考下述数据填空和回答问题:
| MgO | Al2O3 | MgCl2 | AlCl3 | |
| 熔点/℃ | 2852 | 2072 | 714 | 190(2.5×105Pa) |
| 沸点/℃ | 3600 | 2980 | 1412 | 182.7 |
(2)2001年曾报道,硼镁化合物刷新了金属化合物超导温度的最高记录.该化合晶体结构中的晶胞如图1所示.镁原子间形成正六棱柱,六个硼原子位于棱柱内.
则该化合物的化学式可表示为
(3)写出Cu+的核外电子排布式
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(5)某喹喏酮类药物(中心离子是Cu2+)结构如图2,关于该药物的说法正确的是
A.中心离子Cu2+的配位数是5
B.N原子均采用sp2杂化
C.存在配位键、极性共价键和非极性共价键
D.熔点很高,硬度很大.

(12分) 诺贝尔物理学奖曾授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。
则分子中B原子杂化轨道的类型为 ▲ ,同层分子间的主要作用为 ▲ 。
(2)K3[Fe(CN)6]晶体中含有的化学键类型为 ▲ ,Fe3+与CN-之间能够形成化学键的原因是 ▲ 。
(3)等物质的量的氧化物MO与SiC的电子总数相等,则M2+离子的核外电子排布式为 ▲ 。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,晶体中与每个M2+等距离且最近的几个O2-所围成的空间几何构型为 ▲ 。MO的熔点比CaO的高,原因是 ▲ 。
查看习题详情和答案>>