摘要:10.在3C+SiO22CO↑+SiC的反应中.还原剂与氧化剂的物质的量之比是 ( ) A.3∶1 B.1∶3 C.1∶2 D.2∶1
网址:http://m.1010jiajiao.com/timu3_id_150460[举报]
(中国古代四大发明之一--黑火药,它的爆炸反应为:2KNO3+3C+S
A+N2↑+3CO2↑(已配平)
①除 S 外,上列元素的电负性从大到小依次为
②生成物中,A 的电子式为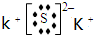
 ,含极性共价键的分子的中心原子轨道杂化类型
,含极性共价键的分子的中心原子轨道杂化类型
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布式为
(3)与N2互为等电子体的分子和离子有(各写一个)
查看习题详情和答案>>
| ||
①除 S 外,上列元素的电负性从大到小依次为
O>N>C>K
O>N>C>K
;②生成物中,A 的电子式为


sp
sp
;③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
1:1
1:1
.(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布式为
3d84s2
3d84s2
,Q2+的未成对电子数是4
4
.(3)与N2互为等电子体的分子和离子有(各写一个)
CO
CO
,CN-
CN-
(限用第二周期的元素表示)在2A+B?3C+5D反应中,表示该反应速率最快的是( )
| A、v(A)═0.5 mol/(L?s) | B、v(B)═0.3mol/(L?s) | C、v(C)═0.8 mol/(L?s) | D、v(D)═1mol/(L?s) |
(2012?唐山二模)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJ?mol-1
(1)已知:
①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489kJ?mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ?mol-1
则a=
(2)在T℃时,该反应的平衡常数K=64,在体积均为2L的恒容密闭容器甲和乙中,分别按下所示加入物质,反应经过一段时间后达到平衡.
①甲容器中CO的平衡转化率为
②下列说法正确的是
a.增加Fe2O3的量可以提高CO的转化率
b.甲、乙容器中CO的平衡转化率之比大于1
c.甲、乙容器中,CO的平衡浓度之比为2:3
d.若容器内气体密度恒定时,标志反应达到平衡状态
(3)实验室有提纯后的铁矿粉(含氧化铁、氧化亚铁中的一种或两种),请设计实验探究其成分:
实验室仅提供如下仪器和试剂:烧杯、试管、玻璃棒、药匙、胶头滴管、酒精灯、试管夹;3mol/L H2SO4溶液、0.01mol/L KMnO4溶液、20% KSCN溶液、蒸馏水.
①提出合理假设:
假设1:只含氧化亚铁;
假设2:只含氧化铁;
假设3:
②请在下列表格中填写实验步骤、预期现象与结论.(可不必填满)
查看习题详情和答案>>
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=akJ?mol-1
(1)已知:
①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489kJ?mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ?mol-1
则a=
-28.5
-28.5
kJ?mol-1,炼铁反应平衡常数K随温度升高而减小
减小
(填“增大”、“不变”或“减小”).(2)在T℃时,该反应的平衡常数K=64,在体积均为2L的恒容密闭容器甲和乙中,分别按下所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲 | 1.0mol | 1.0mol | 1.0mol | 1.0mol |
| 乙 | 1.0mol | 2.0mol | 1.0mol | 1.0mol |
60%
60%
.②下列说法正确的是
cd
cd
(填字母).a.增加Fe2O3的量可以提高CO的转化率
b.甲、乙容器中CO的平衡转化率之比大于1
c.甲、乙容器中,CO的平衡浓度之比为2:3
d.若容器内气体密度恒定时,标志反应达到平衡状态
(3)实验室有提纯后的铁矿粉(含氧化铁、氧化亚铁中的一种或两种),请设计实验探究其成分:
实验室仅提供如下仪器和试剂:烧杯、试管、玻璃棒、药匙、胶头滴管、酒精灯、试管夹;3mol/L H2SO4溶液、0.01mol/L KMnO4溶液、20% KSCN溶液、蒸馏水.
①提出合理假设:
假设1:只含氧化亚铁;
假设2:只含氧化铁;
假设3:
既含氧化亚铁又含氧化铁
既含氧化亚铁又含氧化铁
.②请在下列表格中填写实验步骤、预期现象与结论.(可不必填满)
| 实验操作 | 预期现象及结论 |
| 步骤1:取少量样品于烧杯中加适量稀硫酸溶解 | \ |
| 步骤2: 取少量步骤1所得溶液于试管中滴加几滴KSCN溶液 取少量步骤1所得溶液于试管中滴加几滴KSCN溶液 |
若溶液变红则证明样品中含氧化铁 若不变红则证明样品中不含氧化铁 若溶液变红则证明样品中含氧化铁 若不变红则证明样品中不含氧化铁 |
| 步骤3: 另取少量步骤1所得溶液于试管中滴加几滴KMnO4溶液 另取少量步骤1所得溶液于试管中滴加几滴KMnO4溶液 |
若KMnO4溶液紫色褪去则证明样品中含氧化亚铁 若KMnO4溶液不褪色则证明样品中不含氧化亚铁 若KMnO4溶液紫色褪去则证明样品中含氧化亚铁 若KMnO4溶液不褪色则证明样品中不含氧化亚铁 |
| 步骤4: 空 空 |
空 空 |
 2MgO+Si
2MgO+Si SiF4
SiF4 2CO↑+SiC
2CO↑+SiC