摘要:某工厂每天烧掉100t含硫0.96%的烟煤.为防止SO2污染环境.用生石灰吸收SO2.最终转化为石膏.试计算理论上每年可生成石膏多少吨?
网址:http://m.1010jiajiao.com/timu3_id_149116[举报]
(2012?绵阳模拟)含硫化氢的工业废气要经过治理方能排放,既回收硫单质又防止大气污染.请根据如下治理方法回答相关问题.
(1)电解法治理硫化氢的工艺流程如下:
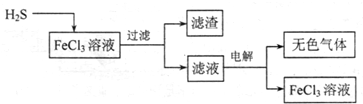
①FeCl3溶液吸收H2S的生成物是
②用惰性电极电解滤液时,阴极的电极反应式为
(2)富玛克斯法治理硫化氢的方法和步骤如下:
a.用2%?3%的Na2CO3溶液吸收含H2S的废气,反应生成2种酸式盐;
b.向上述反应所得溶液中加入液体R-NO(R表示一种芳香烃基),发生如下反应:R-NO+NaHS+H2O→R-NHOH+NaOH+S↓
C.步骤b生成的NaOH在溶液中与另一种酸式盐反应生成正盐;
d.R-NHOH与空气中的氧气反应又得到R-NO.
①写出上述a、c两步反应的离子方程式
②在上述治理硫化氢的全过程中,总反应的化学方程式是
(3)上述两种治理方法的共同优点是
查看习题详情和答案>>
(1)电解法治理硫化氢的工艺流程如下:

①FeCl3溶液吸收H2S的生成物是
FeCl2、HCl和S(或答氯化亚铁、盐酸和硫单质)
FeCl2、HCl和S(或答氯化亚铁、盐酸和硫单质)
②用惰性电极电解滤液时,阴极的电极反应式为
2H++2e-═H 2↑
2H++2e-═H 2↑
,电解总反应的离子方程式是2Fe2++2H+
2Fe3++H 2↑
| ||
2Fe2++2H+
2Fe3++H 2↑
| ||
(2)富玛克斯法治理硫化氢的方法和步骤如下:
a.用2%?3%的Na2CO3溶液吸收含H2S的废气,反应生成2种酸式盐;
b.向上述反应所得溶液中加入液体R-NO(R表示一种芳香烃基),发生如下反应:R-NO+NaHS+H2O→R-NHOH+NaOH+S↓
C.步骤b生成的NaOH在溶液中与另一种酸式盐反应生成正盐;
d.R-NHOH与空气中的氧气反应又得到R-NO.
①写出上述a、c两步反应的离子方程式
CO32-+H2S═HS-+HCO3-
CO32-+H2S═HS-+HCO3-
、HCO3-+OH-═CO32-+H 2O
HCO3-+OH-═CO32-+H 2O
.②在上述治理硫化氢的全过程中,总反应的化学方程式是
2H 2S+O 2
2S↓+2H 2O
| ||
2H 2S+O 2
2S↓+2H 2O
,若某工厂每天需要处理含H2S 10%的废气1800m3,在步骤d中理论上消耗空气
| ||
450
450
m3(空气中O2的体积百分含量以20%计算,所有气体体积均在标准状况下测得).(3)上述两种治理方法的共同优点是
吸收剂可循环使用
吸收剂可循环使用
.含硫化氢的工业废气要经过治理方能排放,既回收硫单质又防止大气污染.请根据如下治理方法回答相关问题.
(1)电解法治理硫化氢的工艺流程如下:
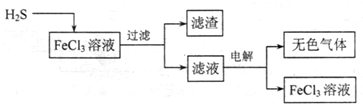
①FeCl3溶液吸收H2S的生成物是______
②用惰性电极电解滤液时,阴极的电极反应式为______,电解总反应的离子方程式是______
(2)富玛克斯法治理硫化氢的方法和步骤如下:
a.用2%?3%的Na2CO3溶液吸收含H2S的废气,反应生成2种酸式盐;
b.向上述反应所得溶液中加入液体R-NO(R表示一种芳香烃基),发生如下反应:R-NO+NaHS+H2O→R-NHOH+NaOH+S↓
C.步骤b生成的NaOH在溶液中与另一种酸式盐反应生成正盐;
d.R-NHOH与空气中的氧气反应又得到R-NO.
①写出上述a、c两步反应的离子方程式______、______.
②在上述治理硫化氢的全过程中,总反应的化学方程式是______,若某工厂每天需要处理含H2S 10%的废气1800m3,在步骤d中理论上消耗空气______m3(空气中O2的体积百分含量以20%计算,所有气体体积均在标准状况下测得).
(3)上述两种治理方法的共同优点是______.
查看习题详情和答案>>
(1)电解法治理硫化氢的工艺流程如下:

①FeCl3溶液吸收H2S的生成物是______
②用惰性电极电解滤液时,阴极的电极反应式为______,电解总反应的离子方程式是______
(2)富玛克斯法治理硫化氢的方法和步骤如下:
a.用2%?3%的Na2CO3溶液吸收含H2S的废气,反应生成2种酸式盐;
b.向上述反应所得溶液中加入液体R-NO(R表示一种芳香烃基),发生如下反应:R-NO+NaHS+H2O→R-NHOH+NaOH+S↓
C.步骤b生成的NaOH在溶液中与另一种酸式盐反应生成正盐;
d.R-NHOH与空气中的氧气反应又得到R-NO.
①写出上述a、c两步反应的离子方程式______、______.
②在上述治理硫化氢的全过程中,总反应的化学方程式是______,若某工厂每天需要处理含H2S 10%的废气1800m3,在步骤d中理论上消耗空气______m3(空气中O2的体积百分含量以20%计算,所有气体体积均在标准状况下测得).
(3)上述两种治理方法的共同优点是______.
含硫化氢的工业废气要经过治理方能排放,既回收硫单质又防止大气污染.请根据如下治理方法回答相关问题.
(1)电解法治理硫化氢的工艺流程如下:
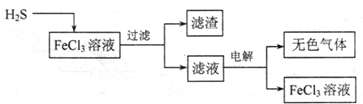
①FeCl3溶液吸收H2S的生成物是______
②用惰性电极电解滤液时,阴极的电极反应式为______,电解总反应的离子方程式是______
(2)富玛克斯法治理硫化氢的方法和步骤如下:
a.用2%?3%的Na2CO3溶液吸收含H2S的废气,反应生成2种酸式盐;
b.向上述反应所得溶液中加入液体R-NO(R表示一种芳香烃基),发生如下反应:R-NO+NaHS+H2O→R-NHOH+NaOH+S↓
C.步骤b生成的NaOH在溶液中与另一种酸式盐反应生成正盐;
d.R-NHOH与空气中的氧气反应又得到R-NO.
①写出上述a、c两步反应的离子方程式______、______.
②在上述治理硫化氢的全过程中,总反应的化学方程式是______,若某工厂每天需要处理含H2S 10%的废气1800m3,在步骤d中理论上消耗空气______m3(空气中O2的体积百分含量以20%计算,所有气体体积均在标准状况下测得).
(3)上述两种治理方法的共同优点是______.
查看习题详情和答案>>
(1)某工厂每天要烧掉含硫1.6%的烟煤200 t,排放出的SO2会严重污染环境,如果变废为宝,将这些SO2回收利用,那么理论上每年(按365 d计)可生产98%的浓硫酸 吨;
(2)若要在铁制件表面镀镍,则镍应与电源的 极相连,电镀液可以用硫酸镍溶液,电镀过程中硫酸镍溶液的浓度会 (填“增大”“减小”或“不变”);
(3)工业上制造水泥、玻璃时都要用到的原料是 (填编号),用所选原料制玻璃的化学方程式是 ;
A.纯碱 B.熟石灰C.石灰石D.黏土
(4)炼铁和炼钢过程的主要区别是 ?????????????????????????????????????????????? ;
(5)明矾净化水的原理是 ????????????????????????????????????????????????????????????????????
(用离子方程式表示);具有暂时硬度的水中除去Mg2+的方法是 ???????????????????????????????????????????????????????? 、
???????????????? ??????????????????????????????????????????? (用化学方程式表示)。
查看习题详情和答案>>