摘要:宝丰一高2005-2006学年上学期第二次月考答题卷 高一化学2006.9
网址:http://m.1010jiajiao.com/timu3_id_148970[举报]
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑
B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.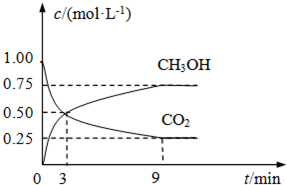
①从3min到9min,v(H2)=
②能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
下列说法正确的是
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
查看习题详情和答案>>
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
C
C
A.电解水制氢:2H2O
| ||
B.高温使水分解制氢:2H2O
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| 高温 |
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

①从3min到9min,v(H2)=
0.125
0.125
mol?L-1?min-1.②能说明上述反应达到平衡状态的是
D
D
(填编号).A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
AC
AC
.A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
自2003年以来,中国、日本和越南相继爆发禽流感,随后禽流感又在全球蔓延,并造成多人死亡.世界卫生组织警告说,禽流感对人类的潜在威胁要远大于“非典”,可能导致全球经济大幅度的衰退.2005年瑞士罗氏制药公司介绍了抗禽流感药物“达菲”的生产工艺.合成“达菲”的重要中间体为莽草酸.为研究莽草酸的分子结构,人们设计如下实验:
(1)莽草酸是一种有机物,其相对分子质量不超过200,是一种白色粉末,易溶于水,难溶于氯仿和苯.取一定量样品燃烧,产物只有CO2和H2O且有n(CO2):n(H2O)=7:5,消耗的O2和生成的CO2的物质的量相等,则莽草酸的分子式为 .
(2)以下是以莽草酸为原料合成有机物B和D的路线:

据此判断莽草酸分子中含有的官能团的名称: , , .
查看习题详情和答案>>
(1)莽草酸是一种有机物,其相对分子质量不超过200,是一种白色粉末,易溶于水,难溶于氯仿和苯.取一定量样品燃烧,产物只有CO2和H2O且有n(CO2):n(H2O)=7:5,消耗的O2和生成的CO2的物质的量相等,则莽草酸的分子式为
(2)以下是以莽草酸为原料合成有机物B和D的路线:

据此判断莽草酸分子中含有的官能团的名称:
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑
B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)CO2可转化成有机物实现碳循环.将2molCO2和6molH2充入容积为3L的密闭容器中,在一定温度和压强条件下发生了下列反应:CO2(g)+3H2 (g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.反应在2分钟时达到了平衡.
①用H2与CO2浓度的变化表示该反应的速率,以它们的速率表示反应达到平衡的关系式是
②达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图1所示,关于温度(T)和压强(P)的关系判断正确的是
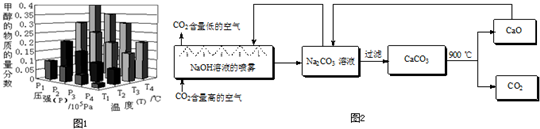
A.P3>P2 T3>T2
B.P2>P4 T4>T2
C.P1>P3 T1>T3
D.P1>P4 T2>T3
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平
衡常数:
下列说法正确的是
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高
(4)二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如图2).
以CO2与NH3为原料可合成化肥尿素[CO(NH2)2].已知:
2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-159.47kJ?mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.49kJ?mol-1
H2O(l)=H2O(g)△H=+88.0kJ?mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式
查看习题详情和答案>>
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
C
C
:A.电解水制氢:2H2O
| ||
B.高温使水分解制氢:2H2O
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| ||
(2)CO2可转化成有机物实现碳循环.将2molCO2和6molH2充入容积为3L的密闭容器中,在一定温度和压强条件下发生了下列反应:CO2(g)+3H2 (g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.反应在2分钟时达到了平衡.
①用H2与CO2浓度的变化表示该反应的速率,以它们的速率表示反应达到平衡的关系式是
3υ(CO2)正=υ(H2)逆
3υ(CO2)正=υ(H2)逆
.②达到平衡时,改变温度(T)和压强(P),反应混合物中CH3OH的“物质的量分数”变化情况如图1所示,关于温度(T)和压强(P)的关系判断正确的是
CD
CD
(填序号).
A.P3>P2 T3>T2
B.P2>P4 T4>T2
C.P1>P3 T1>T3
D.P1>P4 T2>T3
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平
衡常数:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
AC
AC
.A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高
(4)二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如图2).
以CO2与NH3为原料可合成化肥尿素[CO(NH2)2].已知:
2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-159.47kJ?mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.49kJ?mol-1
H2O(l)=H2O(g)△H=+88.0kJ?mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98kJ?mol-1
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98kJ?mol-1
. 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如下图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如下图所示.有关该化合物的叙述正确的是( )
查看习题详情和答案>>
(1)恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示.(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6KJ?mol- 1),请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式: .
②△H2= KJ?mol-1
③在相同条件下,充入1molSO3和0.5mol的O2则达到平衡时SO3的转化率为 ;此时该反应 (填“放出”或“吸收”) kJ的能量.
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
①有效“减碳”的手段之一是节能,下列制氢方法最节能的是 (填序号)
A.电解水制氢:2H2O
2H2↑+O2↑
B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
②CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)浓度随时间变化如上图2所示.从3min到9min,v(H2)= mol?L-1?min-1.
③能说明上述反应达到平衡状态的是 (填编号).
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:下列说法正确的是 .
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
查看习题详情和答案>>

①写出能表示硫的燃烧热的热化学方程式:
②△H2=
③在相同条件下,充入1molSO3和0.5mol的O2则达到平衡时SO3的转化率为
(2)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
①有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O
| ||
B.高温使水分解制氢:2H2O
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| ||
②CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)浓度随时间变化如上图2所示.从3min到9min,v(H2)=
③能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:下列说法正确的是
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.