摘要:6.从铝土矿制备铝的工艺流程: Al 2O3 NaAlO2 Al(OH)3 Al 2O3 Al ⑴请依次写反应的化学方程式 ① ② ③ ④ ⑵请写上述属①②的离子方程式 ① ② ⑶电解加入冰晶石的作用是
网址:http://m.1010jiajiao.com/timu3_id_148319[举报]
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质.
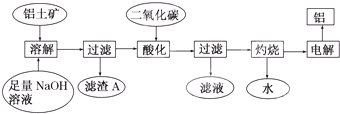
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式 ,滤渣A的主要成分为 .
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 ,通入过量的二氧化碳时,生成沉淀的离子方程式为 .
(3)电解氧化铝,每生成1molAl时,生成 g氧气.
查看习题详情和答案>>
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质.

回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是
(3)电解氧化铝,每生成1molAl时,生成
 铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O═Na2Al2Si2O8↓+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液操作中发生反应的离子方程式:
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
;SiO2+2OH-═SiO32-+H2O
SiO2+2OH-═SiO32-+H2O
.(2)滤渣A的主要成分为
Fe2O3、Na2Al2Si2O8
Fe2O3、Na2Al2Si2O8
;滤渣A的用途是作炼铁的原料(或作生产硅酸盐产品的原料)
作炼铁的原料(或作生产硅酸盐产品的原料)
(只写一种);实验室过滤时使用玻璃棒,其作用是引流
引流
.(3)在工艺流程第三步中,选用二氧化碳作酸化剂的原因是
将NaAlO2完全转化为Al(OH)3
将NaAlO2完全转化为Al(OH)3
.(4)若将铝溶解,下列试剂中最好选用
B
B
(填编号).理由是铝与浓硫酸在常温下发生钝化,加热溶解会产生有毒气体SO2,原料利用率低,而稀硝酸能溶解铝但会产生NO气体,污染空气,硝酸利用率低,但铝与稀硫酸反应速率较快,产生的H2对空气无污染
铝与浓硫酸在常温下发生钝化,加热溶解会产生有毒气体SO2,原料利用率低,而稀硝酸能溶解铝但会产生NO气体,污染空气,硝酸利用率低,但铝与稀硫酸反应速率较快,产生的H2对空气无污染
.A.浓硫酸 B.稀硫酸 C.稀硝酸.
(8分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。
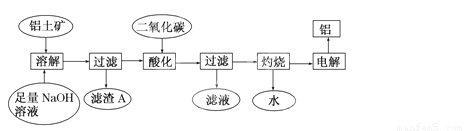
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式 ,滤渣A的主要成分为 。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为 _______ 。
(3)电解氧化铝,每生成1molAl时,生成 g氧气。
查看习题详情和答案>>