摘要:Cl2+2KI=2KCl+I2 2.CaCO3+2HCl= CaCl2+CO2↑+H2O
网址:http://m.1010jiajiao.com/timu3_id_146878[举报]
根据所给的4个反应,判断下列4种物质的氧化性由强到弱的正确顺序是( )
(1)Cl2+2KI=2KCl+I2(2)2FeCl2+Cl2=2FeCl3(3)2FeCl3+2HI=2FeCl2+2HCl+I2(4)H2S+I2=S↓+2HI.
(1)Cl2+2KI=2KCl+I2(2)2FeCl2+Cl2=2FeCl3(3)2FeCl3+2HI=2FeCl2+2HCl+I2(4)H2S+I2=S↓+2HI.
查看习题详情和答案>>
(2011?上海)电解饱和食盐水的反应为2NaCl+2H2O
Cl2↑+H2↑+2NaOH.
(1)在上述方程式上标出电子转移的方向和数目
 .
.
(2)该反应中被氧化的元素是
(3)电解产物氯气既能作氧化剂,也能作还原剂.下列反应中氯气只作氧化剂的是
a.Cl2+2KI→2KCl+I2 b.Cl2+2NaOH→NaCl+NaClO+H2O
c.CuCl2
Cl2↑+Cu d.3Cl2+2Fe
2FeCl3.
查看习题详情和答案>>
| 通直流电 |
(1)在上述方程式上标出电子转移的方向和数目


(2)该反应中被氧化的元素是
Cl
Cl
.阴极产物之一为H2,阴极上发生的变化为还原
还原
反应(选填“氧化”、“还原”).(3)电解产物氯气既能作氧化剂,也能作还原剂.下列反应中氯气只作氧化剂的是
ad
ad
(填写编号).a.Cl2+2KI→2KCl+I2 b.Cl2+2NaOH→NaCl+NaClO+H2O
c.CuCl2
| 通直流电 |
| 点燃 |
某小组准备在实验室中制取干燥、纯净的氯气并验证氯气的性质,设计了如下的实验装置图:
(一) 制取纯净的氯气
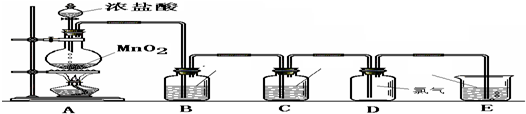
(1)写出A中反应的化学方程式:
(2)B中加入的物质是:
(3)C中加入的物质是:
(4)E中反应方程式为:
(二) 验证氯气的性质:
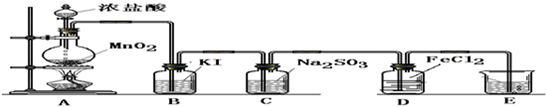
(1)B中发生反应的方程式为:
(2)C中发生反应的方程式为:
(3)D中的反应方程式为:
查看习题详情和答案>>
(一) 制取纯净的氯气

(1)写出A中反应的化学方程式:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)B中加入的物质是:
饱和食盐水
饱和食盐水
作用是:除去Cl2中混有的HCl气体
除去Cl2中混有的HCl气体
.(3)C中加入的物质是:
浓硫酸
浓硫酸
作用是:干燥Cl2
干燥Cl2
.(4)E中反应方程式为:
2NaOH+Cl2 =NaCl+NaClO+H2O
2NaOH+Cl2 =NaCl+NaClO+H2O
.(二) 验证氯气的性质:

(1)B中发生反应的方程式为:
Cl2+2KI=2KCl+I2
Cl2+2KI=2KCl+I2
.(2)C中发生反应的方程式为:
Cl2+Na2SO3+H2O=Na2SO4+2HCl
Cl2+Na2SO3+H2O=Na2SO4+2HCl
.(3)D中的反应方程式为:
2FeCl2+Cl2=2FeCl3
2FeCl2+Cl2=2FeCl3
.